Batas ng ideyal na gas
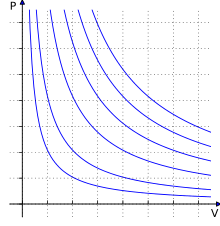
Ang batas ng ideyal na gas (Ingles, ideal gas law) ay ang tumbasan ng estado (equation of state) ng isang hipotetikal na ideyal na gas. Mainam itong gamitin sa maraming mga uri ng gas sa iba-ibang kondisyon ngunit mayroon pa rin itong mga limitasyon. Una itong isinaad ni Émile Clapeyron noong 1834 bilang isang kumbinasyon ng mga empirikal na batas ni Boyle, batas ni Charles, at batas ni Avogadro.[1]
Kadalasang isinusulat ang batas na ito bilang
kung saan ang:
- ay ang presyon ng gas,
- ay ang bolyum ng gas,
- ay ang dami ng gas (sa mole),
- ay ang ideal na konstant ng gas,
- ay ang ganap na temperatura ng gas.
Maaari ring makuha ang batas ng ideyal na gas mula sa teoryang kinetiko ng gas, na nagawa nang hiwalay nina August Krönig noong 1856[2] at Rudolf Clausius noong 1857.[3]
Tumbasan[baguhin | baguhin ang wikitext]
Ang estado ng isang dami ng gas ay natutukoy sa pamamagitan ng presyon, bolyum, at temperatura nito. Ang mga makabagog anyo ng tumbasang ito ay inuugnay ang mga ito sa dalawang anyo.
Ganap na temperatura ang ginagamit sa tumbasang ideal gas; kelvin ang naaangkop na yunit ng SI.[4]
Anyong karaniwan[baguhin | baguhin ang wikitext]
Ang pinakamadalas na ipinakilalang anyo ay
kung saan ang:
- ay ang presyon ng gas,
- ay ang bolyum ng gas,
- ay ang dami ng gas (sa mole),
- ay ang ideal na konstant ng gas,
- ay ang ganap na temperatura ng gas.
Sa yunit na SI, ang P ay sinusukat sa pascal, V ay sinusukat sa kubiko metro, n ay sinusukat sa mole, at T sa kelvin. Ang halaga ng R ay 8.314 J/(K·mol) ≈ 2 cal/(K·mol), o 0.08206 L·atm/(mol·K).
Anyong molar[baguhin | baguhin ang wikitext]
Maaaring tukuyin kung gaano karami ang gas sa pamamagitan ng masa imbis na sa mole. Kaya naman maaaring ibahin ang pagkakasulat ng batas ng ideyal na gas upang mas madali itong gamitin. Ang dami ng kemikal sa yunit na mole n ay katumbas ng masang m (sa gramo) na hinati sa masang molar M (sa gramo kada mole):
Gamit ito, maaaring palitan ang n sa tumbasang ideyal na gas. Pagkatapos ay mapapalitan ang m/V ng densidad ρ:
Kapaki-pakinabang ang anyong ito dahil naiuugnay nito ang presyon, densidad, at temperatura nang hindi kinakailangan ang dami ng gas.
Statistical mechanics[baguhin | baguhin ang wikitext]
Makukuha ang sumusunod na tumbasan mula sa statistical mechanics, ab initio:
kung saan ang P ay ang ganap na presyon ng gas, ang N ay ang bilang ng mga molekula sa isang binigay na bolyum V, ang kB ay ang konstant ni Boltzmann na iniuugnay ang temperatura at enerhiya, at T ay ang ganap na temperatura.
Mga aplikasyon sa termodinamikong mga proseso[baguhin | baguhin ang wikitext]
Ang isang termodinamikong proseso ay isang sistema na gumagalaw mula sa isang estado patungo sa isa pa. Sa talahanayan sa ilalim, ang mga estado ay naka-subscript. Tulad ng ipinapakita sa unang kolumn ng talahanayan, ang mga pangunahing termodinamikong proseso ay natutukoy kung alin sa mga katangian ng gas (P, V, T, o S) ang hindi nagbabago sa buong proseso.
| Proseso | Halagang di-nagbabago | Alam na ratio | P2 | V2 | T2 |
|---|---|---|---|---|---|
| Isobaric na proseso | P2 = P1 | V2 = V1(V2/V1) | T2 = T1(V2/V1) | ||
| P2 = P1 | V2 = V1(T2/T1) | T2 = T1(T2/T1) | |||
| Isochoric na proseso | P2 = P1(P2/P1) | V2 = V1 | T2 = T1(P2/P1) | ||
| P2 = P1(T2/T1) | V2 = V1 | T2 = T1(T2/T1) | |||
| Isothermal na proseso | P2 = P1(P2/P1) | V2 = V1/(P2/P1) | T2 = T1 | ||
| P2 = P1/(V2/V1) | V2 = V1(V2/V1) | T2 = T1 | |||
| Isentropic na proseso | P2 = P1(P2/P1) | V2 = V1(P2/P1)(−1/γ) | T2 = T1(P2/P1)(γ − 1)/γ | ||
| P2 = P1(V2/V1)−γ | V2 = V1(V2/V1) | T2 = T1(V2/V1)(1 − γ) | |||
| P2 = P1(T2/T1)γ/(γ − 1) | V2 = V1(T2/T1)1/(1 − γ) | T2 = T1(T2/T1) | |||
| Polytropic na proseso |
P2 = P1(P2/P1) | V2 = V1(P2/P1)(-1/n) | T2 = T1(P2/P1)(n - 1)/n | ||
| P2 = P1(V2/V1)−n | V2 = V1(V2/V1) | T2 = T1(V2/V1)(1−n) | |||
| P2 = P1(T2/T1)n/(n − 1) | V2 = V1(T2/T1)1/(1 − n) | T2 = T1(T2/T1) |
^ a. Sa isang isentropic na proseso, ang entropy (S) ng sistema ay hindi nagbabago. Sa gayong kundisyon, P1 V1γ = P2 V2γ, kung saan γ ay tinukoy bilang ang rasyo ng kapasidad ng init, na iisa para sa isang perpektong gas. Ang mga halaga nito ay karaniwang 1.4 para sa mga diatomikong mga gas tulad ng nitroheno (N2) at oksiheno (O2), (at hangin, na kung saan 99% ay diatomikong gas). Para naman sa mga monatomikong gas tulad ng mga mariringal na mga hanging (noble gas) elyo (He) at argon (Ar), ang halaga ng γ ay 1.6. Sa isang combustion engine, naglalaro ang halaga ng γ sa pagitan ng 1.35 at 1.15 depende sa lamang gas at temperatura.
Paglayo sa pagiging ideyal ng mga tunay na gas[baguhin | baguhin ang wikitext]
Ang batas ng ideyal na gas ay nararapat lamang gamitin sa mga ideyal na gas, o kaya naman para sa mga totoong gas na gumagalaw tulad ng isang ideyal na gas.
Sa katotohanan, maraming iba't ibang klase ng tumbasan ng estado. Dahil hindi isinasaalang-alang sa batas ng ideal na gas ang laki ng molekula at ang mga interaksyon sa pagitan ng mga ito, ang batas na ito ay pinakatama para sa mga monatomikong gas sa matataas na temperatura at mabababang presyon.
Mga sanggunian[baguhin | baguhin ang wikitext]
- ↑ Clapeyron, E (1834). "Mémoire sur la puissance motrice de la chaleur". Journal de l'École Polytechnique (sa wikang Pranses). XIV: 153–90.
{{cite journal}}: More than one of|authorlink=at|author-link=specified (tulong)CS1 maint: date auto-translated (link) - ↑ Krönig, A. (1856). "Grundzüge einer Theorie der Gase". Annalen der Physik und Chemie (sa wikang Aleman). 99 (10): 315–22. Bibcode:1856AnP...175..315K. doi:10.1002/andp.18561751008.
{{cite journal}}: More than one of|DOI=at|doi=specified (tulong); More than one of|authorlink=at|author-link=specified (tulong)CS1 maint: date auto-translated (link) - ↑ Clausius, R. (1857). "Ueber die Art der Bewegung, welche wir Wärme nennen". Annalen der Physik und Chemie (sa wikang Aleman). 176 (3): 353–79. Bibcode:1857AnP...176..353C. doi:10.1002/andp.18571760302.
{{cite journal}}: More than one of|DOI=at|doi=specified (tulong); More than one of|authorlink=at|author-link=specified (tulong)CS1 maint: date auto-translated (link) - ↑ "Equation of State". Inarkibo mula sa ang orihinal noong 2014-08-23. Nakuha noong 2016-11-25.
{{cite web}}: CS1 maint: date auto-translated (link)











