AIDS
| HIV/AIDS | |
|---|---|
| Klasipikasyon at mga panlabas na sanggunian | |
 Ang pulang laso ay isang simbolo ng pagkakaisa ng mga taong positibo sa HIV at sa mga taong namumuhay na may AIDS. | |
| ICD-10 | Bb20.htm+ b20 20 . – Bb20.htm+ b24 24 . |
| ICD-9 | 042-044 |
| OMIM | 609423 |
| DiseasesDB | 5938 |
| MedlinePlus | 000594 |
| eMedicine | emerg/253 |
| MeSH | D000163 |
Ang Human immunodeficiency virus infection / Acquired immunodeficiency syndrome (HIV/AIDS) ay isang sakit ng sistemang immuno ng tao na sanhi ng HIV.[1] Sa simulang impeksiyon, ang isang taong nahawaan ay maaaring makaranas ng isang maikling yugto ng tulad ng trangkasong (influenza) mga sakit. Ito ay karaniwang sinusundan ng isang humabang panahong walang mga sintomas. Habang nagpapatuloy ang sakit na ito, ito ay mas nanghihimasok sa sistemang immuno ng indibidwal na gumagawa sa mga meron nito na mas malamang na magkaroon ng mga impeksiyon kabilang ang mga oportunistikong impeksiyon at mga tumor na karaniwang hindi dumadapo sa mga taong may gumaganang sistemang immuno.
Ang HIV ay pangunahing naisisalin sa pamamagitan ng hindi ligtas na pakikipagtalik, nahawaang dugo at mga karayom at sa ina tungo sa anak sa pagbubuntis, panganganak o pagpapasuso.[2] Ang ilang mga pluido sa katawan gaya ng laway at luha ay hindi nagpapasa ng HIV.[3] Ang pag-iwas sa impeksiyon ng HIV na pangunahin sa pamamagitan ng ligtas na pakikipagtalik (paggamit ng kondom) at mga programang pagpapalit ng karayom sa mga gumagamit ng droga ay isang mahalagang stratehiya upang makontrol ang pagkalat ng sakit na ito.
Sa kasalukuyan ay walang gamot (cure) o bakuna upang mapuksa ang virus na HIV sa katawan ng mga taong nahawaan nito. Gayunpaman, ang terapiyang antiretroviral ay maaaring magpabagal ng sakit at maaaring tumungo sa isang malapit sa normal na pagtagal ng buhay sa mga nahawaan nito. Bagaman ang paggamot antiretroviral ay nagpapabawas ng panganib ng kamatayan at mga komplikasyon mula sa sakit, ang mga gamot na ito ay mahal at maaaring maiugnay sa mga side effect.
Ang pagsasaliksik henetiko ay nagpapakitang ang HIV ay nagmula sa Kanlurang-sentral na Aprika noong simula nang ika-20 siglo.[4] Ang AIDS ay unang nakilala ng Centers for Disease Control and Prevention (CDC) ng Estados Unidos noong 1981 at ang sanhi nitong HIV ay natukoy sa simulang bahagi nang dekada.[5] Simula pagkakatuklas nito, ang AIDS ay nagsanhi ng halos 30 milyong mga kamatayan (mula 2009).[6] Mula 2010, ang tinatayang mga 34 milyong katao ang nahawaan ng HIV sa buong mundo.[7] Ang AIDS ay itinuturing na isang pandemikong sakit na umiiral sa malaking sakop ng mundo at aktibong kumakalat.[8] Ang HIV/AIDS ay may malaking epekto sa lipunan bilang sakit at pinagmumulan ng diskriminasyon. Ang sakit na ito ay mayroon ring malaking epekto sa ekonomiya.
Klasipikasyon[baguhin | baguhin ang wikitext]
| Species | Birulensiya | Paghawa | Paglaganap | Pinagpalagay na pinagmulan |
|---|---|---|---|---|
| HIV-1 | Mataas | Mataas | Pandaigdigan | Chimpanzee |
| HIV-2 | Mababa | Mababa | Kanlurang Aprika | Sooty Mangabey |
Ang HIV ay kasapi ng genus na Lentivirus,[9] na kasapi ng pamilyang Retroviridae.[10] Ang mga Lentiviruse ay nag-aangkin ng maraming mga karaniwang mga katangiang morpolohikal at biolohikal. Maraming mga espesye ay nahahawaan ng lentivirus na mailalarawang responsable sa pangmatagalang mga sakit na may mahabang yugtong inkubasyon.[11] Ang mga Lentivirus ay naipapasa bilang may isang-hibla, positibong-senso na nakatakip na mga virus na RNA. Sa pagpasok sa inaasintang selula, ang viral na genome ng RNA ay kinokonberte (kabaligtarang transkripsiyon) sa dalawang-hiblang DNA ng isang kinokodigong viral na kabaligtarang transcriptase na inihahatid sa kahabaan ng viral genome sa partikulong virus. Ang nagreresultang viral DNA ay ipinapasok naman sa nucleus ng selula at isinasama sa selular na DNA ng kinokodigong viral na integrase at mga kapwa-paktor na hosto.[12] Kapag ito ay naisama na, ang virus ay maaaring maging latento na pumapayag sa virus at mga selulang hosto nito na makaiwas sa pagkakatuklas (detection) ng sistemang immuno. Sa alternatibong paraan, ang virus ay maaring tinranskriba na lumilikha ng bagong mga genome na RNA at mga protinang viral na kinakahon at inilalabas mula sa selula habang ang mga bagong partikulong virus na nagpasimula ng replikasyon (pagkopya) ay bagong sumiklo.
Ang dalawang mga uri ng HIV ay inilalarawan na: HIV-1 at HIV-2. Ang HIV-1 ang virus na naunang natuklasan at pinangalanang LAV at HTLV-III. Ito ay mas birulente, mas nakahahawa,[13] at ang sanhi ng karamihan sa mga impeksiyong HIV sa buong mundo. Ang mas mababang nakakahawang HIV-2 kumpara sa HIV-1 ay nagpapahiwatig na ang mas kaunti sa mga nalantad sa HIV ay mahahawaan kada paglalantad. Dahil sa relatibong mahinang kakayahan nito sa pagpasa, ang HIV-2 ay karamihang nakalagak lamang sa Kanlurang Aprika.[14]
Mga tanda at sintomas[baguhin | baguhin ang wikitext]
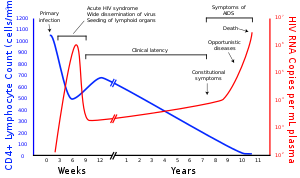
Ang impeksiyon o pagkahawa ng HIV-1 ay kaugnay ng patuloy na pagbaba ng bilang ng CD4+ na selulang T at pagdagdag ng bigat na viral na lebel ng HIV sa dugo. Ang yugto ng impeksiyon ay maaaring matukoy sa pamamagitan ng pagsukat ng bilang ng CD4+ na selulang T at bigat na viral ng pasyente.
Ang mga yugto ng impeksiyong HIV ay impeksiyong acute (na kilala rin bilang pangunahing impeksiyon), latensiya at AIDS. Ang impeksiyong acute ay tumatagal ng ilang mga linggo at maaaring kabilangan ng mga sintomas gaya ng lagnat (fever), lymphadenopathy (pamamaga ng kulani), pharyngitis (masakit na lalamunan o sore throat), rash, myalgia (kirot sa masel), malaise, at mga singaw sa bibig at lalamuna. Ang yugtong latensiya ay sumasangkot sa kaunti o walang mga sintomas at maaaring tumagal mula 2 linggo hanggang 20 taon o higit pa depende sa indibidwal. Ang panghuling yugto ng pagkahawa ng HIV ang AIDS. Ito ay inilalarawan ng mababang bilang ng CD4+ na selulang T (mas kaunti sa 200 kada mikrolitro) at paglitaw ng iba't ibang mga oportunistikong impeksiyon, kanser at iba pang mga kondisyon.
Ang maliit na lebel ng mga impektado ng HIV-1 na indibidwal ay nagpapanatili ng mataas na lebel ng mga CD4+ na selulang T nang walang terapiyang antiretroviral. Gayunpaman, ang karamihan sa mga ito ay may natutuklasan (detectable) na bigat na viral at kalaunan ay tumutuloy sa AIDS nang walang paggamot bagaman mas mabagal sa iba. Ang mga indibidwal na ito ay inuuri bilang kontroler ng HIV o pangmatagalang hindi tagatuloy (long-term nonprogressors o LTNP). Ang mga indibiwal na nagpapanataili ng bilang ng CD4+ ng selulang T at mayroon ring mababa at hindi matutuklasang bigat na viral nang walang paggamot ng antiretroviral ay tinatawag na mga elitistang kontrol o mga elitistang tagasupil (ES).[15][16]
Impeksiyong acute[baguhin | baguhin ang wikitext]
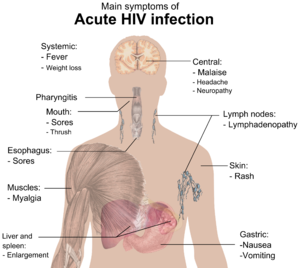
Ang impeksiyong HIV ay pangkalahatang nangyayari sa pagpapakilala ng mga pluidong pangkatawan mula sa impektado indibidwal (indibidwal na may HIV) tungo sa katawan ng isang indibidwal na hindi impektado (indibidwal na walang HIV). Ang isang yugto ng mabilisang replikasyong viral ay nagreresulta, na nagdudulot sa pagsagana ng virus sa periperal na dugo. Sa yugto ng pangunahing impeksiyon, ang lebel ng HIV ay maaaring umabot ng ilang mga milyong partikulo ng virus kada mililitro ng dugo.[17]
Ang dugong ito ay sinasamahan ng maliwanag na pagbagsak ng bilang ng mga sumisirkulong CD4+ na selulang T. Ang acute na viremia na ito ay iniuugnay sa halos lahat ng mga pasyente sa aktibasyon (pagpapagana) ng CD8+ na mga selulang T na pumapatay ng mga selulang impektado ng HIV at kalaunan ng produksiyon ng antibody o seroconversion. Ang dugong CD8+ na selulang T ay ipinagpapalagay na mahalaga sa pagkokontrol ng mga lebel ng virus na sumusukdol (peak) at pagkatapos ay bumabagsak habang ang bilang ng CD4+ selulang T ay muling tumataas. Ang isang mabuting dugong CD8+ na selulang T ay inigunay sa mas mabagal na pagpapatuloy ng sakit at isang mas mabuting prognosis bagaman ito ay hindi nagtatanggal ng virus.[18]
Sa yugtong ito (na karaniwang ay 2–4 linggo pagkatapos ng pagkakalantad), maraming mga indibidwal ay nagkakaroon ng influenza o tulad ng mononucleosis na sakit na tinataag na acute HIV infection na ang pinakaraniwang mga sintomas ay kinabibilangan ng lagnatlymphadenopathy, pharyngitis, rash, myalgia, malaise at mga singaw sa bibig at lalamunan, at maaari ring kabilangan ng mas hindi karaniwang sakit sa ulo, nausea, at pagsusuka, lumaking atay/spleen, pagbawas ng timbang, thrush, at mga neurolohikal na sintomas. Ang mga impektadong indibidwal ay maaaring makaranas ng lahat o ilan o wala sa mga sintomas na ito. Ang tagal ng mga sintomas ay nag-iiba iba na ang aberahe ay 28 araw at karaniwan ay tumatagal ng hindi bababa sa isang linggo.[19]
Dahil sa mga hindi spesipikong kalikasan ng mga sintomas na ito, ang mga ito ay kadalasang hindi nakikilala bilang mga tanda ng impeksiyong HIV. Kahit pa ang mga pasyente ay pumunta sa kanilang mga doktor o hospital, ang mga ito ay kadalasang nabibigyan ng maling diagnosis na merong may isa sa mas karaniwang mga nakahahawang sakit na may parehong mga sintomas. Dahil dito, ang mga pangunahing sintomas na ito ay hindi ginagamit sa pagda-diagnos ng impeksiyong HIV dahil ang mga ito ay hindi nakikita sa lahat ng mga kaso at dahil sa marami sa mga ito ay sinasanhi ng ibang mas karaniwang mga sakit. Gayunpaman, ang pagkilala ng sindroma ay mahalaga dahil ang pasyente ay mas nakahahawa sa yugtong ito.
Impeksiyong kroniko[baguhin | baguhin ang wikitext]
Ang isang malakas ng pagtatanggol ng sistemang immuno ay nagbabawas ng mga partikulong virus sa daluyang ng dugo na naghuhudyat ng pagsisimula ng pangalawa o kronikong (chronic) impeksiyong HIV. Ang pangalawang yugto ng impeksiyong HIV ay iba iba mula 2 linggo hanggang 20 taon. Sa yugtong ito ng impeksiyon, ang HIV ay aktibo sa mga kulani na karaniwan ay patuloy ang pamamaga bilang tugon sa malaking mga halaga ng virus na nabitag (trapped) sa follicular na dendritikong selulang network.[21] Ang mga nakapaligid na tisyu na mayaman sa CD4+ na selulang T ay maaari ring maging impektado at ang mga partikulong viral ay natitipon sa parehong mga impektadong selula at bilang malayang virus. Ang mga indibidwal na nasa yugtong ito ay nakahahawa pa rin. Sa panahong ito, ang CD4+ CD45RO+ na selulang T ay nagdadala ng karamihan sa mga bigat na proviral.[22]
Sa yugtong ito ng impeksiyon, ang unang pagsisimula ng terapiyang antiretroviral ay malaking nagpapaigi ng pagpapatuloy (survival) ng buhay ng indibidwal na may HIV kumpara sa mga indibidwal na may ipinagpalibang terapiya.
AIDS[baguhin | baguhin ang wikitext]
Kapag ang bilang ng CD4+ na selulang T ay bumagsak na mas mababa sa kritikal na antas ng 200 selula kada mililitro, ang pinamamagitang selulang immunidad ay nawawala at ang mga impeksiyon na may iba ibang oportunistikong mikrobyo ay lumilitaw. Ang unang mga sintomas ay karaniwang kinabibilangan ng katamtaman at hindi maipaliwanag na pagbawas ng timbang, paulit ulit na impeksiyon sa traktong respiratoryo (gaya ng sinusitis, bronchitis, otitis media, pharyngitis), prostatitis, skin rashes, at mga singaw sa bibig.
Ang mga karaniwang oportunistikong mga impeksiyon at tumor na ang ang karamihan ay kinokontrol ng masaganang CD4+ ang pinamamagitan ng selulang T na immunidad ay nagsisimulang makaapekto sa pasyente. Sa karaniwang ang resistansiya ay nawawala sa simula sa pambibig na espesye ng Candida at Mycobacterium tuberculosis, na tumutungo sa karagdagang pagiging marupok sa pambibig na candiasis (thrush) at tubercolosis. Sa kalaunan, ang muling pagpapagana ng latentong herpes viruses ay maaaring magsanhi ng paglala ng muling paglitaw ng herpes simplex eruptions, shingles, Epstein-Barr virus-induced B-cell lymphomas, o Kaposi's sarcoma.
Ang Pneumonia na sanhi ng fungus na Pneumocystis jirovecii ay karaniwan at kalimitang nakamamatay. Sa mga huling yugto ng AIDS, ang impeksiyon sa cytomegalovirus (na isa pang herpes virus) o Mycobacterium avium complex ay mas nakikita. Hindi lahat ng mga pasyenteng may AIDS ay nakakakuha ng lahat ng mga impeksiyong ito o tumor at mayroong mga ibang tumor at impeksiyon na hindi gaanong makikita ngunit mahalaga pa rin.
Transmisyon (Pagpasa)[baguhin | baguhin ang wikitext]
| Ruta ng kalantaran | Tinatantiyang mga impeksiyon kada 10,000 na kalantaran sa impektado o may sakit na indibidwal |
|---|---|
| Transpusyon o pagsasalin ng dugo | 9,000 (90%)[25] |
| Ina-sa-anak kabilang ang pagbubuntis, panganganak at pagpapasuso (nang walang paggamot sa HIV) | 2,500 (25%)[26] |
| Ina-sa-anak kabilang ang pagbubuntis, panganganak at pagpapasuso (nang may kanais nais na paggamot sa HIV) | 100–200 (1%–2%)[26] |
| Pagsasalo sa paggamit sa karayom o siringhe sa paggamit ng droga. | 67 (0.67%)[27] |
| Percutaneous (o pambalat) na pagtusok ng impektadong karayom | 30 (0.30%)[28] |
| Tumatanggap na pakikipagtalik na anal (2009 at 2010 na mga pag-aaral) | 170 (1.7%)‡ [30–890][29] / 143 [48–285][24] |
| Tumatanggap na pakikipagtalik na anal (batay sa data ng 1992 na pag-aaral) | 50 (0.5%)[30][31] |
| Pumasok na na pakikipagtalik na anal para sa mga hindi tuling lalake (2010 pag-aaral) | 62 (0.62%)a [7–168][24] |
| Pumasok na na pakikipagtalik na anal para sa mga tuling lalake (2010 pag-aaral) | 11 (0.11%)a [2–24][24] |
| Pumasok na na pakikipagtalik na anal (batay sa 1992 pag-aaral) | 6.5(0.065%)[30][31] |
| Mababang-sahod na bansa babae-sa-lalake | 38 (0.38%)‡ [13–110][29] |
| Mababang-sahod na bansa lalake-sa-babae | 30 (0.3%)‡ [14–63][29] |
| Babaeng tumatanggap ng pakikipagtalik sa puke | 10 (0.1%)[30][31][32] |
| Lalakeng nagpasok ng titi nito sa pakikipagtalik sa puke | 5 (0.05%)[30][31] |
| Paggamit ng bibig sa titi ng lalake | 1 (0.01%)†b[31] |
| Lalakeng ginamitan ng bibig sa titi nito | 0.5 (0.005%)†b[31] |
- a Natuklasan ng ilang pag-aaral ang hindi sapat na ebidensiya na ang pagtutuli sa mga lalake ay pumoprotekta sa impeksiyong HIV sa mga lalakeng nakikipagtalik sa kapwa lalake.[33][34]
- b Ang trauma o pinsala sa bibig, mga singaw, pamamaga, sabay na umiiral na mga sakit na naipapasa sa pakikipagtalik, ehakulasyon sa bibig at sistemikong pagsupil ng immuno ay maaaring magpadagdag ng rate ng pagpasa ng HIV.[35]
- † "pinakamahusay na hulang pagtatantiya"
- ‡ Tinipong probabilidad na pagtatantiya ng pagpasa.
- Ang naka-bracket na mga halaga ay kumakatawan sa 95% na konpidensiyang interbal.
Ang datos na ipinapakita sa itaas ay kumakatawan sa transmisyon (pagpasa) nang walang gamit na kondom. Ang panganib ay malaking dumadagdag sa presensiya ng mga ulcer sa ari (genital), mga hiwa sa mukosa, sabay na umiiral na mga sakit na naipapasa sa pakikipagtalik, o pakikipagtalik sa katalik na may may taas na bigat na viral ng HIV. [36] Ang pagkakalantad sa prostitusyon at ang antas ng pambansang kita ay maaaring makaapekto sa panganib.[29]
Ang tatlong pangunahing mga ruta ng transmisyon ng HIV ay natukoy. Ang HIV-2 ay naipapasa ng hindi gaanong kadalas sa pamamagitan ng rutang ina-sa-anak at rutang pakikipagtalik kesa sa HIV-1.
Seksuwal[baguhin | baguhin ang wikitext]

Ang karamihan sa mga impeksiyong HIV ay nakukuha sa pamamagitan ng hindi ligtas o hindi protektadong pakikipagtalik (hindi paggamit ng kondom). Ang pagkawalang bahala sa HIV ay gumagampan ng mahalagang papel sa panganib ng pagkuha ng HIV.[kailangan ng sanggunian] Ang transmisyon sa pakikipagtalik ay nangyayari kung ang isang impektado ng HIV na mga pluidong inilalabas sa katawan ng isang impektado ng HIV na indibidwal ay dumikit o napunta sa mga membrano ng ari (sex organ), bibig o rectum ng taong katalik nito na walang sakit na HIV. Sa mga may mataas na sahod na bansa, ang panganib sa babae-sa-lalakeng transmisyon ay 0.04% kada akto ng pakikipagtalik at 0.08% transmisyon kada akto ng pakikipagtalik sa lalake-sa-babae. Sa iba't ibang mga dahilan, ang mga rate na ito ay 4 hanggang 10 mga beses na mas mataas sa may mababang-sahod na mga bansa.[29] Ang rate para sa tumatanggap na pakikipagtalik na anal ay mas matas na 1.7% kada akto ng pakikipagtalik.[29]
Ang isang 1999 na meta-analisis ng mga pag-aaral ng paggamit ng kondom ay nagpakitang ang konsistenteng paggamit ng latex na kondom ay nagbabawas ng panganib ng transmisyong seksuwal ng HIV na mga 85%.[37] Gayunpaman, ang spermicide ay maaaring aktuwal na magpadagdag ng rate ng transmisyon.[38][39][40]
Ang mga randomang kinontrol na mga pagsubok medikal kung saan ang mga hindi tuling lalake ay randomang itinakda na tuliin sa mga kondisyong malinis at binigyan ng pagpapayo at ibang mga lalakeng hindi natuli ay isinagawa sa Timog Aprika,[41] Kenya,[42] and Uganda[43] na nagpapakita ng pagbabawas ng transmisyon ng HIV sa babae-sa-lalakeng pakikipagtalik na mga respektibong 60%, 53%, at 51%. Bilang resulta nito, ang isang lupon ng mga eksperto ng World Health Organization (WHO) at UNAIDS Secretariat ay "nagrekomiyenda na ang pagtutuli sa mga kalalakihan ay makilala bilang karagdagang mahalagang interbensiyon sa pagbabawas ng panganib ng nakukuhang HIV sa pakikipagtalik na heteroseksuwal sa mga lalake."[44] Sa mga lalakeng nakikipagtalik sa kapwa lalake, walang sapat na ebidensiya na ang pagtutuli sa mga lalake ay pumoprotekta laban sa impeksiyong HIV o iba pang mga sakit na naipapasa sa pakikipagtalik.[33]
Ang mga pag-aaral ng HIV sa mga babaeng sumailalim sa pagputol ng pambabaeng ari ay nag-ulat ng magkahalong mga resulta na ang ilang ebidensiya ay nagpapakita ng dumagdag na panganib ng transmisyon.[45][46][47][48] Ang mga programang naglalayon na humikayat ng pangingilin (abstinence) sa pakikipagtalik samantalang humihikayat at nagtuturo ng mga stratehiya ng ligtas na pakikipagtalik para sa mga aktibong seksuwal na indibidwal ay maaaring magbawas ng panandalian o pangmatagalang pag-aasal na nakapapanganib sa HIV sa mga kabataan sa may mataas-na-sahod na mga bansa ayon sa 2007 pag-aaral na Cochrane Review.[49]
Mga produkto ng dugo[baguhin | baguhin ang wikitext]
Sa pangkalahatan, kung ang isang impektado ng HIV na dugo ay dumikit o tumungo sa anumang bukas na sugat, ang HIV ay maaaring maipasa sa indibidwal na walang HIV. Ang rutang ito ng transmisyon ay sumasaalang alang sa mga impeksiyon sa mga tagagamit ng itinuturok na droga, at tumatanggap ng pagsasalin ng dugo (bagaman ang karamihan sa mga pagsasalin ng dugo ay sinusuri para sa HIV sa mga maunlad na bansa) at mga produkto ng dugo. Ito ay ikinababahala rin para sa mga taong tumatanggap ng pangangalagang medikal sa mga rehiyong kung saan may laganap na mababang uring kalinisan ng katawan (hygiene) sa paggamit ng panturok na mga kasangkapan gaya ng muling paggamit ng mga karayom sa mga bansang Ikatlong Daigdig (third world). Ang mga manggagawa ng pangangalagang kalusugan gaya ng mga nars, manggagawa ng laboratoryo at doktor ay nahawaan din bagaman ito ay bihirang mangyari. Simula na makikilala ang transmisyon ng HIV sa pamamagitan ng dugo, ang mga personnel na medikal ay inaatasang magprotekta sa kanilang mga sarili mula sa pagdikit o paglapit sa mga dugo sa pamamagitan ng pangkalahatang mga pag-iingat. Ang mga taong nagbibigay at tumatanggap ng tato (tattoo), mga pagtuturok sa katawan (body piercing) at pagsusugat sa katawan (scarification) ay maaaring manganib sa impeksiyong HIV. Natagpuan ang HIV na mababa ang konsentransiyon sa laway, luha at ihi ng mga impektado ng HIV na indibidwal ngunit walang mga naitalang kaso ng impeksiyon sa mga pluidong inilalabas na ito at ang potensiyonal ng transmisyon ay hindi mahalaga.[50] Hindi posible para sa mga lamok na magpasa ng HIV.[51]
Ina-sa-anak[baguhin | baguhin ang wikitext]
Ang transmisyon ng HIV virus mula sa ina sa anak ay maaaring mangyari in utero (habang nagbubuntis), intrapartum (sa panganganak), o sa pamamagitan ng pagpapasuso. Sa kawalan ng paggamot, ang rate ng transmisyon hanggang sa kapanganakan ng sanggol mula ina hanggang sa sanggol ay 25%.[26] Gayunpaman, kung may makukuhang kombinasyon ng paggamot ng drogang antiretroviral at seksiyong Caesarian ay magbabawas ng panganib sa HIV na kasingbaba ng isang porsiyento.[26] Ang pagkatapos ng kapangakang transmisyon mula sa ina tungo sa anak ay malaking maiiwasan sa pamamagitan ng kumpletong pag-iwas sa pagpapasuso sa sanggol. Gayunpaman, ang paraang ito ay may malaking kaugnayan sa morbidad (pagkakaroon ng sakit). Ang eksklusibong pagpapasuso at ang probisyon ng pinalawig na antiretroviral prophylaxis sa sanggol ay epektibo rin sa pag-iwas ng transmisyon.[52] Ang UNAIDS ay nagtantiyang ang mga 430,000 bata ay nahawaan ng HIV sa buong mundo noong 2008(19% ng lahat ng mga bagong impeksiyon) na pangunahin sa rutang ito at ang karagdagang mga 65,000 na impeksiyon ay naiwasan sa pamamagitan ng pagbibigay ng antiretroviral prophylaxis sa mga kababaihang positibo-sa-HIV .[53]
Pangmaramihang impeksiyon[baguhin | baguhin ang wikitext]
Hindi tulad ng ilang mga virus, ang impeksiyong HIV ay hindi nagbibigay ng karagdagang immunidad laban sa mga karagdagang impeksiyon, sa partikular ay sa kaso ng mga virus na may mas malayong pagkakatulad sa gene . Ang parehong inter- at intra-clade na pangmaramihang mga impeksiyon ay naiulat,[54] at naiugnay pa sa mas mabilis na pagpapatuloy ng sakit.[55] Ang pangmaramihang mga impeksiyon ay mahahati sa dalawang mga kategorya na batay sa panahon ng pagkakamit ng ikalawang strain. Ang kapwa impeksiyon (coinfection) ay tumutukoy sa dalawang mga strain na lumalabas na nakuha sa parehong panahon (o kasing magkatulad upang makilala ng hiwalay). Ang muling impeksiyon (o superimpeksiyon) ang impeksiyong may ikalawang strain sa isang masusukat na panahong pagkatapos ng unang strain. Ang parehong mga anyo ay naiulat para sa HIV sa parehong acute at kronikong impeksiyon sa buong mundo.[56][57][58][59]
Pag-iwas[baguhin | baguhin ang wikitext]
Ang isang kurso ng paggamot na antiretroviral na agad na nilapat pagkatapos ng pagkalantad sa HIV ay tumutukoy sa pagkatapos ng pagkalantad na prophylaxis ay nagpapabawas ng panganib ng impeksiyon kung sinimulan nang mabilis hangga't maaari.[60] Noong Hulyo 2010, ang isang gel na pang-puke ng tao na naglalaman ng tenofovir na isang tagapigil ng baliktad na transcriptase ay naipakitang nagpabawas ng rate ng impeksiyon ng HIV ng 39 porsiyento sa isang pagsubok na isinagawa sa Timog Aprika.[61] Ang simulang paggamot gamit ang terapiyang antiretroviral ng mga taong nahawaan ng HIV ay pumrotekta sa 96% ng mga partner nito mula sa impeksiyon.[62] Ang pagsusuring pagkatapos ng pagkalantad sa HIV ay nirerekomiyenda sa pasimula, sa ika-anim na linggo, ikatlong buwan at ika-anim na buwan.[63]
Sa kasalukuyan ay walang alam na makukuha ng publikong bakuna ng HIV para sa HIV o AIDS.[64][65][66] Gayunpaman, ang isang bakuna na kombinasyon ng dalawang nakaraang hindi matagumpay na mga kandidatong bakuna na ALVAC-HIV at AIDSVAX ay iniulat noong Seytembre 2009 na nagresulta sa 30% pagbabawas sa mga impeksiyon sa isang pagsubok medikal na isinagawa sa Thailand.[67][68] Ang mga karagdagang pagsubok ng bakuna ay nagpapatuloy sa kasalukuyan.[69][70]
Virolohiya[baguhin | baguhin ang wikitext]
Istraktura at Genome[baguhin | baguhin ang wikitext]
Ang HIV ay iba sa istraktura sa iba pang mga retrovirus. Ito ay tinatayang sperikal[71] na may diametrong mga 120 nm na mga 60 beses na mas maliit sa selulang pulang dugo ngunit malaki para sa isang virus.[72] Ito ay binubuo ng dalawang mga kopya ng positibong isang-hiblang RNA na nagkokodigo para sa siyam na gene ng virus na sinarhan ng konikal na capsid na binubuo ng 2,000 mga kopya ng protinang viral na p24.[73] Ang isang-hiblang RNA ay masikip na binibigkis sa mga protinang nucleocapsid na p7 at mga ensaym na kailangan sa kaunlaran ng virion gaya ng baliktad na transcriptase, proteases, ribonuclease at integrase. Ang isang matriks na binubuo ng protinang viral na p17 ay pumapaligid sa capsid na sumisiguro sa integridad o kabuuan ng partikulong virion.[73]
Ito naman ay napapaligiran ng viral na envelope na binubuo ng dalawang mga patong ng matabang mga molekulang tinatawag na phospholipid na kinuha mula sa membrano ng selula ng tao kung ang bagong nabuong partikulong virus ay sumanga mula sa selula. Ang nakabigkis sa mga viral envelope ang mga protina mula sa selula ng hosto at mga 70 kopya ng kompleks na protinang HIV na umuungas sa ibabaw ng partikulong virus.[73] Ang protinang ito na kilala bilang Env, ay binubuo ng isang cap na gawa sa tatlong mga molekulang tinatawag na glycoprotein (gp) 120, at isang sangang binubuo ng tatlong mga molekulang gp41 na kumakabit sa istraktura ng viral envelope.[74] Ang kompleks na glycoprotein na ito ay pumapayag sa virus na kumabit at sumanib sa mga inaasintang selula upang magpasimula ng nakahahawang siklo.[74] Ang parehong mga pang-ibabaw na protinang ito lalo na ang gp120 ay itinuturing na mga inaasinta (targets) ng panghinaharap na paggamot o mga bakuna laban sa HIV.[75]
Ang genome na RNA ay binubo ng hindi bababa sa mga pitong istraktural na tanda (LTR, TAR, RRE, PE, SLIP, CRS, and INS), at siyam na gene na (gag, pol, at env, tat, rev, nef, vif, vpr, vpu, at misan ay pangsampung tev, na pagsasanib ng tat env and rev) na nagkokodigo sa 19 mga protina. Tatlo sa mga gene na ito na gag, pol, at env ay naglalaman ng impormasyon na kailangan upang gumawa ng mga istraktural na protina para sa mga bagong partikulong virus.[73] Halambawa, ang env ay nagkokodigo para sa protinang tinatawag na gp160 na sinisira ng viral na ensaym upang bumuo ng gp120 at gp41. Ang mga anim na natitirang gene na tat, rev, nef, vif, vpr, at vpu (o vpx sa kaso ng HIV-2) ay mga regulatoryong gene para sa mga protinang kumokontrol sa kakayahan ng HIV na makahawa ng mga selula, lumikha ng mga bagong kopya ng virus (replikasyon) o magsanhi ng sakit.[73]
Ang dalawang mga protinang Tat (p16 ay p14) ang mga transkripsiyonal na transaktibidator para sa tagataguyod na LTR na kumikilos sa pamamagitan ng pagbibigkis ng elementong TAR RNA. Ang TAR ay maaari ring iproseso sa microRNA na rumiregula sa mga gene ng apoptosis na ERCC1 at IER3.[76][77] Ang protinang Rev (p19) ay sangkot sa paglilipat ng RNA mula sa nucleus ng selula at cytoplasmo sa pamamagitan ng pagbibigkis ng RRE elementong RNA. Ang protinang Vif (p23) ay pumipigil sa aksiyon ng APOBEC3G (na isang protinang selula na nagde-deaminado ng DNA: mga hybrid na RNA at/o nanghihimasok sa protinang Pol). Ang protinang Vpr (p14) ay pumipigil sa paghahati ng selula sa G2/M. Ang protinang Nef (p27) ay babang-nagreregula ng CD4 (ang pangunahing reseptor na viral) gayundin ang mga molekulang MHC class I at class II.[78][79][80]
Ang Nef ay nakikipag-ugnayan rin sa mga sakop na SH3. Ang protinang Vpu (p16) ay umiimpluwensiya sa paglabas ng bagong mga partikulong virus mula sa mga impektadong selula.[73] Ang mga dulo ng bawat hibla ng HIV RNA ay naglalaman ng sekwensiyang RNA na tinatawag na mahabang terminal na pag-ulit (long terminal repeat o LTR). Ang mga rehiyon sa LTR ay kumikilos na mga switch upang kontrolin ang produksiyon ng mga bagong virus at maaaring pumukaw ng mga proteina mula sa HIV o sa selulang hosto. Ang elementong Psi ay sangkot sa pagkakahon ng viral genome at nakikilala ng mga protinang Gag at Rev. Ang elementong SLIP (TTTTTT) ay sangkot sa paglipatbalangkas sa Gag-Pol na bumabasa ng balangkas na kailangan upang makagawa ng gumaganang Pol.[73]
Tropismo[baguhin | baguhin ang wikitext]

Ang terminong tropismong viral ay tumutukoy sa kung aling mga uri ng selula ang nahahawaan ng HIV. Ang HIV ay maaaring humawa sa iba't ibang uri ng mga selulang immuno gaya ng CD4+ na mga selulang T, macrophage, at microglial. Ang pagpasok ng HIV-1 sa mga macrophage at CD4+ na mga selulang T ay pinamamagitan sa pamamagitan ng pakikipag-ugnayan ng mga virion envelope glycoprotein (gp120) sa molekulang CD4 sa inaasintang mga selula gayundin sa mga kapwa reseptor na chemokine.[74]
Ang mga strain na macrophage ng HIV-1, o hindi-syncitia-na pumupukaw na mga strain (NSI) ay gumagamit ng reseptor na β-chemokine na CCR5 para sa pagpasok at kaya ay may kakayahang magreplika sa mga macrophage at CD4+ na mga selulang T.[81]
Ang α-chemokine SDF-1 na ligando CXCR4 ay sumusupil ng replikasyon ng mga hiwalay na T-tropic HIV-1. Ginagawa nito ito sa pamamagitan ng ilalim-na-pagreregula ng ekspresyon ng CXCR4 sa ibabaw ng mga selulang ito. Ang HIV na tanging gumagamit ng reseptor na CCR5 ay tinatawag R5; ang mga tanging gumagamit ng CXCR4 ay tinatawag na X4, at ang gumagamit ng parehong ito ay tinatawag na X4R5. Gayunpaman, ang tanging paggamit ng kapwa reseptor ay hindi nagpapaliwanag ng tropismong viral dahil hindi lahat ng virus na R5 ay nakagagamit ng CCR5 sa mga macrophage para sa isang produktibong impeksiyon[81] at ang HIV ay maaari ring makahawa ng pangilalim na uri ng myeloid na dendritikong mga selula,[82] na malamang ay bumubuo ng imbakan na nagpapanatili ng impeksiyon kapag ang bilang ng CD4+ mga selulang T ay labis na bumagsak sa mababang mga lebel.
Ang ilang mga tao ay hindi tinatablan o nahahawaan ng ilang mga strain ng HIV.[83] Halimbawa, ang mga taong may mutasyong CCR5-Δ32 ay resistante (hindi tinatablan) ng impeksiyon ng virus na R5 dahil ang mutasyon ay pumipigil sa HIV na magbigkis sa kapwa reseptor na ito na nagbabawas ng kakahayan nito na humawa ng mga inaasintang selula.
Ang pakikipagtalik ang pangunahing paraan ng transmisyon ng HIV. Ang HIV na X4 at R5 ay makikita sa semilya na ipinapasa mula sa lalake sa katalik nito (babae o lalake). Ang virion ay maaaring humawa ng maraming mga inaasintang selula at kumalat sa buong organismo. Gayunpaman, ang proseso ng pagpili ay tumutungo sa nananaig na transmisyon ng virus na R5 sa daanang ito.[84][85][86] Kung paanong ang selektibong prosesong ito ay kumikilos ay nasa ilalim pa rin ng pagsisiyasat ngunit ang isang modelo ay ang spermatozoa ay maaaring selektibong magdala ng R5 HIV habang kanilang inaangkin ang parehong CCR3 at CCR5 ngunit hindi ang CXCR4 sa kanilang ibabaw[87] at ang selulang epithelial sa ari (genital) ay may kinikilingang sumasamsam sa virus na X4.[88] Sa mga pasyenteng nahawaan ng pangilalim na uri ng B HIV-1, kadalasan ay mayroong switch na kapwa reseptor sa huling yugto ng sakit at ang mga barianto (uri) ng T-tropic ay lumilitaw na maaaring makahawa sa iba ibang mga selulang T sa pamamagitan ng CXCR4.[89] Ang mga uring ito ay nagrereplika naman nang mas agresibo na may tumaas na birulensiya na nagsasanhi ng mabilisang pagkaubos ng selulang T, pagbagsak ng sistemang immuno at mga paglitaw ng mga oportunistikong impeksiyon na naghuhudyat ng pagsisimula ng AIDS.[90] Kaya sa kurso ng impeksiyon, ang pag-aangkop na viral sa paggamit ng CXCR4 imbis ng CCR5 ay maaaring isang mahalagang hakbang sa pagtungo sa AIDS. Ang ilang mga bilang ng pag-aaral ng mga indibidwal na nahawaan ng pang ilalim na uring B ay natukoy na sa pagitan ng 40 at 50% ng mga pasyente ng AIDS ay maaaring magpatira ng mga virus ng SI at ipinagpapalagay ng phenotipong X4.[91][92]
Ang HIV-2 ay mas hindi gaanong patoheniko kesa sa HIV-1 at mas limitado sa pamamahaging pandaigdigan nito. Ang pagkuha ng mga "kasamang genes" ng HIV-2 at ang mas maraming mga parteno ng paggamit ng kapwa reseptor (kabilang ang independiyenteng CD4) ay maaaring makatulong sa virus sa pag-aangkop nito upang makaaiwas sa likas na restriksiyong mga paktor na makikita sa mga selulang hosto. Ang pag-aangkop sa paggamit ng normal na makinaryang selular upang magkaroon ng kakayahang makapagpasa at produktibong impeksiyon ay nakatulong rin sa paglikha ng replikasyon ng HIV-2 sa mga tao. Ang isang stratehiya ng pagpapatuloy (survival) para sa anumang nakahahawang ahente ay hindi pagpatay ng hosto nito kundi sa huli ang pagiging isang commensal na organismo. Sa pagkakamit ng mababang patohenisidad sa paglipas ng panahon, ang mga barianto na mas matagumpay sa pagpasa ay mapipili.[93]
Siklo ng Replikasyon[baguhin | baguhin ang wikitext]

Pagpasok sa selula[baguhin | baguhin ang wikitext]
Ang HIV ay pumapasok sa macrophages at CD4+ na mga selulang T sa pamamagitan ng adsorpsiyon ng mga glycoprotein sa ibabaw sa mga reseptor sa inaasintang selula na sinundan ng pagsasanib ng viral envelope sa membrano ng selula at paglabas ng HIV capsid sa selula.[94][95]
Ang pagpasok sa selula ay nagmumula sa pamamagitan ng interaksiyon ng trimeric envelope complex (gp160 spike) at parehong CD4 at reseptor na chemokine (na pangkalahatan ay CCR5 o CXCR4 ngunit ang iba ay alam na nakikipag-ugnayan) sa ibabaw ng selula.[94][95] Ang gp120 bumibigkis sa integrin α4β7 na nagpapagana ng LFA-1 na sentral na integrin na sangkot sa paglikha ng mga sinapseng virolohikal na nangangasiwa ng mahusay na selula-sa-selulang pagkalat ng HIV-1.[96] Ang gp160 spike ay naglalaman ng mga nagbibigkis na mga sakop (domains) para sa parehong mga reseptor na CD4 at chemokine.[94][95]
Ang unang hakbang sa pagsasanib ay kinasasangkutan ng mataas na apinidad ng pagkakabit ng mga nagbibigkis na sakop (domains) na CD4 ng gp120 sa CD4. Kapag ang gp120 ay nakabigkis na sa protinang CD4, ang envelope complex ay sumasailalim sa isang istraktural na pagbabago na naglalantad ng mga chemokine na nagbibigkis sa mga sakop ng gp120 at pumapayag sa mga ito na makipag-ugnayan sa mga inaasintang reseptor na chemokine.[94][95] Ito ay pumapayag para sa mas matatag na dalawang-umuungos na pagkakabit na pumapayag sa N-terminal na nagsasanib na peptide na gp41 upang makatagos sa membrano ng selula.[94][95] Ang inulit na mga sekwensiya sa gp41, HR1, at HR2 ay nakikipag-ugnayan naman na nagsasanhi ng pagbagsak ng ektraselular na bahagi ng gp41 sa isang hairpin. Ang pulupot na istrakturang ito ay nagpapalapit sa virus at mga membrano ng selula na pumapayag sa pagsasanib ng mga membrano at kalaunang pagpasok ng viral capsid.[94][95]
Pagkatapos ang HIV ay bumigkis sa inaasintang selula, ang RNA ng HIV at iba't ibang mga ensaym kabilang ang baligtad na transcriptrase, integrase, ribonuclease, and protease, ay itinutusok (injected) sa loob ng selula.[94] Habang isinasagawa ang batay sa microtubule na paghahatid sa nucleus, ang viral na isang hiblang RNA genome ay tinranskriba sa dalawang-hibang DNA na isinasama naman sa kromosoma ng hosto.
Ang HIV ay maaaring humawa ng mga selulang dendritiko (DC) sa pamamagitan ng rutang CD4-CCR5 na ito, ngunit ang isa pang ruta gamit ang spesipiko sa mannose na C-uring lectin na mga reseptor gaya ng DC-SIGN ay maaari ring gamitin.[97] Ang mga DC ang isa sa mga unang selula na naeenkwentro ng virus sa pagpasang nangyayari sa pakikipagtalik. Ang mga ito ay kasalukuyang ipinagpapalagay na gumagampan ng mahalagang papel sa pamamaigtan ng pagpasa ng HIV sa mga selulang T kapag ang virus ay nabitig sa mukosa ng mga DC.[97] Ang presensiya ng FEZ-1 na natural na umiiral sa mga neuron ay pinaniniwalaang nagpapaiwas sa impeksiyon ng mga selula ng HIV.[98]
Replikasyon at transkripsiyon[baguhin | baguhin ang wikitext]
Sa madaling panahong pagkatapos na ang viral capsid ay pumasok sa selula, ang isang ensaym na tinatawag na baligtad na transcriptase ay nagpapalaya ng isang-hiblang (+)RNA na genome mula sa ikinabit na mga protinang viral at kumokopya nito sa molekulang complementary DNA (cDNA).[99] Ang proseso ng baligtad na transkripisyon ay labis na nagagawi sa pagkakamali at ang mga nagreresultang mutasyon ay maaaring magsanhi ng resistansiya (hindi pagtalab sa droga) o pumayag sa virus na sumakop sa sistemang immuno ng katawan. Ang baligtad na transcriptase ay mayroon ring aktibidad na ribonuclease na sumisira sa viral RNA habang isinasagawa ang sintesis ng cDNA gayundin ng independiyente sa DNA na aktibidad na DNA polymerase na lumilikha ng sensong DNA mula sa antisensong cDNA.[100] Sa pagiging magkasama, ang cDNA at ang komplementong anyo nito ay bumubuo ng dalawang-hiblang viral DNA na inihahatid naman sa nucleus ng selula. Ang pagsasama ng viral DNA sa genome ng selula ng hosto ay isinasagawa ng isa pang ensaym na viral na tinatawag na integrase.[99]

Ang isinamang viral DNA na ito ay maaaring humimlay ng hindi aktibo sa latentong yugto ng impeksiyong HIV.[99] Upang aktibong lumikha ng virus, ang ilang mga selular na paktor ng transkipsiyon ay hindi kinakailangang umiiral, na ang pinakamahalaga ang NF-κB (NF kappa B) na taas-na-nireregula kapag ang mga selulang T ay naging aktibo.[101] Ang ibig sabihin nito, ang mga selulang malamang na mapatay ng HIV ang mga kasalukuyang lumalaban sa impeksiyon.
Habang nangyayari ang repklikasyon ng virus, ang isinamang DNA provirus ay tintranskriba sa mRNA na pinutol (spliced) sa mas maliit na mga piraso. Ang mga maliit na mga pirasong ito ay inilalabas mula sa nucleus patungo sa cytoplasma kung saan ang mga ito ay isinasalin sa mga regulatoryong protinang Tat (na humihikayat ng bagong produksiyon ng virus) at Rev. Habang ang bagong nalikhang protinang Rev ay nagtitipon sa nucleus, ito ay bumibigkis sa viral mRNAs at pumapayag sa mga hindi naputol (unspliced) RNA na umalis sa nucleus kung saan ang ito ay napananatili hanggang sa maputol.[102] Sa yugtong ito, ang mga istraktural na protinang Gag at Env ay nalilikha mula sa buong habang mRNA. Ang buong-habang RNA ay aktwal na genome ng virus; ito ay nagbibigkis sa protinang Gag at ikinakahon sa mga bagong partikulong virus.
Ang HIV-1 at HIV-2 ay lumalabas na nagkakahong ng kanilang RNA nang magkaiba. Ang HIV-1 ay nagbibigkis sa anumang angkop na RNA samantalang ang HIV-2 ay may kinikilangang nagbibigkis sa mRNA na ginamit upang lumikha ng mismong protinang Gag. Ito ay maaaring mangahulugang ang HIV-1 ay may mas mabuting kakayahan na sumailalim sa mutasyon. Ang impeksiyong HIV-1 ay tumutuloy sa AIDS nang mas mabilis kesa sa impeksiyong HIV-2 at ang
Pagtitipon at paglabas[baguhin | baguhin ang wikitext]
Ang huling hakbang ng siklong viral na pagtitipon ng mga bagong viron na HIV-1, ay nagsisimula sa membranong plasma ng selula ng hosto. Ang poliprotinang Env (gp160) ay dumadaan sa endoplasmikong retikulum at inihahahatid sa kompleks na Golgi kung saan ito ay pinaghihiwalay ng protease at pinoproseso sa dalawang HIV envelope na mga glycoprotein na gp41 at gp120. Ang mga ito ay inihahatid sa membranong plasma ng selula ng hosto kung saan ang gp41 ay nagkakabit sa gp120 sa membrano ng impektadong selula. Ang Gag (p55) at Gag-Pol (p160) na mga polyprotein ay umuugnay rin sa panloob na ibabaw ng membranong plasma kasama ang genomikong RNA ng HIV habang ang nabubuong virion ay nagsisimulang sumanga mula sa selula ng hosto. Ang maturasyon (pagiging hinog o ganap) ay nangyayari sa bumubuong sanga o sa hindi hinog na viron pagkatapos itong sumanga mula sa selula ng hosto. Sa maturasyon, ang HIV proteases ay naghihiwalay ng mga polyprotein sa mga indibidwal na gumaganang protina at ensaym ng HIV. Ang iba't ibang mga istraktural na bahagi ay nagtitipon naman upang lumikha ng hinog (mature) na HIV virion.[103] Ang hakbang na ito ng paghihiwalay ay maaaring mapigil ng mga tagapigil ng protease. Ang hinog (mature) na virus ay may kakayahan namang makahawa ng iba pang selula.
Pagkakaibang henetiko[baguhin | baguhin ang wikitext]

Ang HIV ay iba sa maraming mga virus dahil ito ay may napakataas na henetikong pagkakaiba. Ang pagkakaibang ito o dibersidad ay resulta ng mabilis na replikasyong siklo na may paglikha ng 1010 kada arawa ksasama ng mataas na rate ng mutasyon na mga tinatayang 3 x 10−5 kada nucleotide base kada siklo ng replikasyon at muling pagsasamang mga katangian ng baligtad na transcriptase.[104][105][106]
Ang masalimuot na senaryong ito ay tumutungo sa paglikha ng maraming mga barianto (uri) ng HIV sa isang impektadong pasyente sa kurso ng isang araw.[104] Ang pagiging iba iba nito ay dinagdagan kapag ang isang selula ay sabay na nahawaan ng dalawa o mas maraming mga iba ibang strain ng HIV. Kapag ang sabay sabay na pagkahawa ay nangyari, ang genome ng progeny virion ay maaaring binubuo ng mga hiblang RNA mula sa dalawang magkaibang strain. Ang hybrid na virion ay humahawa naman sa bagong selula kung saan ito sumasailalim sa isang replikasyon. Habang nangyayari ito, ang baligtad na transcriptase sa pamamagitan ng pagtalon ng paurong sulon sa pagitan ng dalawang magkaibang suleras (template) na RNA ay lilikha ng bagong na-sintesis na retroviral sekwensiyang DNA na muling pagsasama sa pagitan ng dalawang mga magulang na genome.[104] Ang muling pagsasamang ito ay pinakahalata kapag ito ay nangyayari sa pagitan ng mga pangilalim na uri.[104]
Ang malapit na kaugnay na simian immunodeficiency virus (SIV) ay nag-ebolve sa maraming mga strain na inuri sa mga natural na species ng hosto. Ang mga SIV strain ng Aprikanong berdeng unggoy (SIVagm) at sooty mangabey (SIVsmm) ay pinaniniwalaang may mahabang kasaysayang ebolusyonaryo sa mga hosto nito. Ang mga hostong ito ay naka-angkop sa presensiya ng virus[107] na makikita sa mataas na mga lebel sa dugo ng hosto ngunit nagpupukaw lamang ng isang katamtamang tugon ng immuno,[108] does not cause the development of simian AIDS,[109] at hindi sumasailalim sa labis na mutasyon at muling pagsasamang tipikal sa impeksiyong HIV sa mga tao.[110]
Salungat dito, kapag ang mga strain ay nakahawa sa mga species ng hayop na hindi naka-angkop sa HIV (mga hostong "heterologous" gaya ng rhesus o cynomologus macaques), ang mga hayop ay bumubuo ng AIDS at ang virus ay lumilikha ng pagkakaiba ibang henetiko katulad ng nakikita sa impeksiyon ng HIV sa tao.[111] Ang Chimpanzee SIV (SIVcpz) na pinakamalapit na kamag-anak ng HIV-1 ay kaugnay ng dumagdag na mortalidad (kamatayan) at tulad ng AIDS na mga sintomas sa mga natural na hosto nito.[112] Ang SIVcpz ay lumalabas na naipasa na relatibong kamakailan lamang sa mga chimpanzee at tao kaya ang mga hosto nito ay hindi pa naka-angkop sa virus.[107] Ang virus na ito ay nakawala rin ng tungkulin ng gene na Nef na makikita sa karamihan ng SIV. Kung wala ang tungkuling ito, ang pagkaubos ng selulang T ay mas malamang na tumutuloy sa kawalang immuno (immunodeficiency).[112]
Ang tatlong mga pangkat ng HIV-1 ay natukoy sa basehan ng mga pagkakaiba sa rehiyong envelope (env) na M, N, and O.[113] Ang pangkat M ang pinakalaganap at nahahati sa walang mga pang-ilalim na uri (o clade batay sa buong genome na heograpikong walang katulad.[114] Ang pinakalaganap ang pangilalim na uring B (na natagpuan ng pangunahin sa Hilagang Amerika at Europa), A at D (na pangunahing natagpuan Aprika) at C (na pangunahing natagpuan sa Aprika at Asya). Ang mga pangilalim na uring ito ay bumubuo ng mga sanga sa phylohenetikong puno na kumakatawan sa angkan ng pangkat M ng HIV-1. Ang kapwa impeksiyon sa mga walang katulad na pangilalim na uri ay nagpapalitawa ng sumisirkulang muling pinagsamang mga anyo (CRF). Noong 2000, ang huling taon kung saan ang analisis ng pandaigdigan paglaganap ng pangilalim ng uri ay nagawa, 47.2% ng pandaigdigang mga impeksiyon ay ng pangilalim na uring C, 26.7% ay ng pangilalim na uring A/CRF02_AG, 12.3% ay ng pangilalim na uring B, 5.3% way ng pangilalim na uring D, 3.2% ay ng pangilalim na uring CRF_AE, at ang natitirang 5.3% at binubuo ng mga ibang pangilalim na uri at CRF.[115] Ang karamihan sa mga pagsasaliksik sa HIV-1 ay nakapokus sa pangilalim na uring B. Kaunting mga laboratoryo lamang ang nakapokus sa ibang mga pangilalim na uri nito.[116] Ang pag-iral ng ika-apat na pangkat na "P" ay hinipotesis batay sa virus na naihiwalay noong 2009.[117][118][119] Ang strain na ito ay maliwanag na hango mula sa gorilla SIV (SIVgor) na unang naihiwalay mula sa western lowland gorilla noong 2006.[117]
Ang henetikong sekwensiya ng HIV-2 ay isang bahagi lamang na homologo sa HIV-1 at mas malapit na katulad ng SIVsmm.
Diagnosis[baguhin | baguhin ang wikitext]
Maraming positibo sa HIV na mga tao ang walang alam na sila ay nahawaan (infected) ng HIV virus. Halimbawa, mababa sa 1% ng mga aktibong seksuwal na populasyong pangsiyudad sa Aprika ang nasubok (tested) at ang proporsiyon na ito ay mas mababasa sa mga rural na populasyon. Sa karagdagan, ang tanging 0.5% ng mga buntis na babaeng pumpupunta sa mga pasilidad pangkalusugan ang napayuhan, nasubok, o nakatanggap ng mga resulta ng pagsubok. Muli, ang proporsiyon na ito ay mas mababa sa mga rural na pasilidad pangkalusugan. Dahil sa ang mga donor ay hindi alam ang kanilang impeksiyon, ang dugo ng donor (nagbigay) at mga produkto ng dugong ginagamit sa medisina at pananaliksik medikal ay rutinang (routinely) ini-screen para sa HIV.
Ang pagsubok (testing) ng HIV-1 ay binubuo ng inisyal na screening sa isang enzyme-linked immunosorbent assay (ELISA) upang matukoy ang mga antibody sa HIV-1. Ang mga specimen na may hindi reaktibong resulta mula sa inisyal na ELISA ay tinuturing na negatibo sa HIV malibang ang bagong pagkakalantad sa isang impektadong katalik na hindi alam na may HIV ay nangyari. Ang mga specimen na may reaktibong resulta ng ELISA, ang resulta ay muling sinusubok (retested) sa duplika (duplicate) Kung ang resulta ng pagsubok na duplika ay reaktibo, ang specimen ay inuulat na paulit ulit na reaktibo at sumasailalim sa isang pagsubok ng pagkokompirma na may spesipikong karagdagang pagsubok, halimbawa ang Western blot o ang hindi mas karaniwang immunofluorescence assay (IFA)). Ang mga tanging specimen na paulit ulit na reaktibo sa ELISA at positibo sa IFA o reaktibo sa Western blot ay itinuturing na positibo sa HIV at indikatibo ng impeksiyon ng HIV. Ang mga specimen na paulit ulit na reaktibo sa ELISA ay paminsan minsang nagbibgay ng hindi matukoy na resulta ng Western blot na maaaring hindi kompletong tugon ng antibody sa HIV ng isang impektadong indibidwal o mga hindi spesipikong raksiyon sa isang hindi impektadong indibidwal.
Bagaman ang IFA ay maaaring gamitin upang kompirmahin ang impeksiyon sa mga ambiguosong (malabong) mga kasong ito, ang assay na ito ay hindi malawak na ginagamit. Sa pangkalahatan, ang ikalawang specimen ay dapat kolektahin ng higit sa isang buwang kalaunan at muling subukin para sa mga indibidwal na may hindi matukoy na resulta ng Western blot. Bagaman hindi gaanong karaniwang makukuha, ang nucleic acid testing (e.g., viral RNA o proviral DNA amplification method) ay maaari ring makatulong sa ilang mga sitwasyon. Sa karagdagan, ang mga specimen ay maaaring magbigay ng hindi konklusibong mga resulta dahil sa mababang kantidad ng specimen. Sa mga sitwasyong ito, ang ikalawang specimen ay kinokolekta at sinusubok para sa impeksiyon ng HIV.
Ang modernong pagsubok HIV ay labis na tiyak (accurate). Ang tsansa ng isang resultang mali-positibo (false positive) sa dalawang-hakbang na protocol ng pagsubok ay tinatantiyang 0.0004% hanggang 0.0007% sa pangkalahatang populasyon sa Estados Unidos.
Pangangasiwa[baguhin | baguhin ang wikitext]
Sa kasalukuyan ay walang gamot (cure) o epektibong bakuna para sa HIV na kumpletong mag-aalis ng virus na HIV sa katawan ng indibidwal na nahawaan nito. Ang pangangasiwa sa mga indibidwal na nahawaan ng HIV ay binubuo ng terapiyang antiretroviral (HAART) na nagpapabagal ng pagpapatuloy ng sakit.[120] Mula 2010, ang higit sa 6 milyong mga indibidwal ay umiinom ng HAART sa may mababa at gitnang sahod na mga bansa.[7]
Terapiyang antiviral[baguhin | baguhin ang wikitext]
Ang kasalukuyang mga opsiyon na HAART ay mga kombinasyon (o cocktail) na binubuo ng hindi bababa sa tatlong mga gamot na kabilang sa hindi bababa sa dalawang uri o klase ng mga ahenteng antiretroviral.[121] Sa simula, ang paggamot ay karaniwang isang hindi-nucleoside na tagapigil ng baligtad na transcriptase (NNRTI) na dinagdagan ng dalawang mga analogong nucleoside ng tagapigil ng baligtad na transcriptase (NNRTI).[121] Ang mga karaniwang NRTI ay kinabibilangan ng zidovudine (AZT) o tenofovir (TDF) at lamivudine (3TC) o emtricitabine (FTC).[121] Ang mga kombinasyon ng mga ahente na kinabibilangan ng isang tagapigil ng protease (PI) ay ginagamit kung ang nasa itaas na rehimen ay nawawalan na ng pagiging epektibo.[121]
Kung kelan sisimulan ang terapiyang antiretrovial ay paksa ng debate.[122][123] Ang parehong World Health Organization, European guidelines at ang Estados Unidos ay nagrerekomiyenda ng mga antiretroviral sa lahat ng mga adolesente, matatandang tao at mga buntis na babae na may bilang ng CD4 na mas mababa sa 350/uL o sa mga may sintomas kahit hindi isasaalang-alang ang bilang ng CD4.[121][122] Ito ay sinusuportahan ng katotohanan na ang pagsisimula ng paggamot sa lebel na ito ay nagpapabawas ng panganib ng kamatayan.[124] Sa karagdagan, inirerekomiyenda rin ng Estados Unidos ang mga ito para sa lahat ng mga indibidwal na nahawaan ng HIV kahit hindi isasaalang alang ng bilang ng CD4 o mga sintomas.[125] Inirerekomiyenda rin ng WHO ang paggamot sa mga kapwa nahawaan ng tubercolosis at sa mga may kronikong aktibong hepatitis B.[121] Kapag nasimulan na ang paggamot ng antiretroviral, nirerekomiyenda na ito ay ituloy nang walang patid o "holidays".[122] Maraming mga tao ay nadiagnos lamang pagkatapos ng pagkakataon na ang kanis nais na paggamot ay dapat simulan.[122] Ang ninanais na kalalabasan ng paggamot ay isang pangmatagalang bilang ng HIV-RNA na mababa sa 50 mga kopya/mL.[122] Ang mga lebel na tinutukoy kung ang paggamot ay epektibo ay inisyal na nirerekomiyenda pagkatapos ng apat na linggo at kapag ang mga lebel ay bumagsak na sa 50 mga kopya/mL, ang mga pagtingin bawat tatlo o anim na buwan ay karaniwang sapat.[122] Ang hindi sapat na kontrol ay itinuturing na mas malaki kesa sa 400 mga kopya/mL.[122] Batay sa mga kriteryang ito, ang paggamot ay epektibo sa higit sa 95% ng mga taong merong HIV sa unang taon.[122]
Ang mga benepisyo ng paggamot ay kinabibilangan ng isang nabawasang panganib ng pagpapatuloy sa AIDS at isang nabawasang panganib ng kamatayan.[126] Sa mga maunlad na bansa, ang paggamot ay nagpapabuti rin ng kalusugang pisikal at pang-isipan ng mga meron nito.[127] Sa paggamot, mayroon isang 70% na nabawasang panganib ng pagtatamo ng tuberculosis.[121] Ang mga karagdagang benepisyo ay kinabibilangan ng isang nabawasang panganib ng pagpasa ng sakit sa mga partner na katalik ng mga indbidwal na may HIV at isang nabawasang pagpasa sa ina-tungo-sa-anak mula sa inang may HIV.[121] Ang pagiging epektibo ng paggamot ay nakasalalay sa isang malaking bahagi sa pagsunod sa terapiyang ito.[122] Ang mga dahilan ng hindi-pagsunod ay kinabibilangan ng mababa o kawalang paglapit (access) sa pangangalagang medical,[128] hindi sapat na mga suportang panlipunan, sakit sa pag-iisip at pang-aabuso ng droga.[129] Gayundin sa pagiging masalimuot ng mga rehimeng paggamot (dahil sa bilang ng mga iniinom na pill at dalas ng pag-inom nito), ang mga epektong adberso ay maaari ring lumikha ng hindi sinasadyang hindi pagsunod dito.[130] Gayunpaman, ang pagsunod ay mabuti sa may mababang sahod na mga bansa gaya ng nasa may mataas na sahod na mga bansa.[131]
Ang mga spesipikong pangyayaring adberso ay nauugnay sa ahenteng iniinom.[132] Ang ilan sa mga relatibong karaniwang epektong ito ang: nauugnay sa HIV na lipodystropiya, dyslipidemia, at diabetes mellitus lalo na sa mga gamot na tagapigil ng protease.[133] Ang ilang mga karaniwang sintomas ay kinabibilangan ng pagtatae[132][134] at isang tumaas na panganib ng sakit na cardiovascular.[135] Gayunpaman, ang mga epektong adberso ay mababa sa mga ilang mas bagong nirerekomiyendang paggamot.[122] Ang gastos ay maaari ring maging isyu dahil sa ang ilang mga gamot na ito ay mahal[136]. Gayunpaman, simula 2010, ang 47% ng mga nangangailangan nito ay umiinom nito sa may mababa at gitnang sahod na mga bansa.[7] Ang ilang mga gamot ay maaaring maiugnay sa mga depekto sa kapanganakan sa mga sanggol ng inang may HIV at kaya ay hindi angkop sa mga babaeng umaasang magkaroon ng anak.[122]
Ang mga rekomendasyon ng paggamot sa mga bata ay medyo iba kesa sa mga matatandang tao. Sa umuunlad na mga bansa simula 2010, ang 23% ng mga batang nangangailangan nito ay mayroong paglapit sa mga gamot na ito.[137] Ang parehong World Health Organization at Estados Unidos ay nagrerekomiyenda ng paggamot para sa lahat ng mga bata na may mababa sa 12 buwan ang edad.[138][139] Nirerekomiyenda ng Estados Unidos sa mga nasa pagitan ng 1 taon at 5 taon na may mga bilang na HIV RNA ng higit sa 100,000 mga kopya/mL at sa mga higit sa 5 taon ng paggamot kapag ang mga bilang ng CD4 ay mababa sa 500/ul.[138]
Mga impeksiyong oportunistiko[baguhin | baguhin ang wikitext]
Ang mga paraan upang maiwasan ang mga impeksiyong oportunistiko ay epektibo sa maraming mga taong may HIV/AIDS. Ang paggamot ng mga antiviral ay kadalasang nagpapabuti ng kasalukuyan gayundin nagpapabawas ng panganib ng panghinaharap na mga impeksiyong oportunistiko. [132] Ang bakuna laban sa hepatitis A at hepatitis B ay ipinapayo sa lahat ng mga tao nasa panganib ng HIV bago sila mahawaan, gayunpaman, ang mga ito ay maaaring bakunahan pagkatapos mahawaan ng HIV.[140] Ang prophylaxis na Trimethoprim/sulfamethoxazole sa pagitan ng apat at anim na linggong taong gulang at pagwawakas ng pagpapasuso sa mga sanggol na ipinanganak sa mga inang positibo sa HIV ay nirerekomiyenda sa mga pagtatakdang nililimitahan ng mga mapagkukunan.[137] Ito ay nirerekomiyenda rin upang maiwasan ang PCP kapag ang bilang ng CD4 sa mga tao ay mababa sa 200 mga selula/uL at sa mga mayroon o nakaraang mayroong PCP.[141] Ang mga taong may malaking immunosuppresyon ay pinapayuhan rin na tumanggap ng terapiyang prophilaktiko para sa toxoplasmosis at Cryptococcus meningitis.[142] Ang mga angkop na nakakaiwas na mga pamamaran ay nagpabawas ng rate ng mga impeksiyong ito nang 50% sa pagitan ng 1992 at 1997.[143]
Medisinang alternatibo[baguhin | baguhin ang wikitext]
Sa Estados Unidos, ang tinatayang 60% ng mga taong may HIV ay gumagamit ng iba't ibang mga uri ng alternatibong medisina.[144] Ang pagiging epektibo ng karamihan ng mga terapiyang ito ay hindi napatunayan.[145] Tungkol sa payong pang-pagkain, may ilang ebidensiya na nagpapakita ng benepisyo sa mga suplemento ng mikronutriento.[146] Ang ebidensiya para sa suplementasyon ng selenium ay halo na ilang mga tentatibong ebidensiya ng benepisyo.[147] May ilang ebidensiya na ang suplementasyon ng bitamina A sa mga bata ay nagpapabawas ng kamatayan at nagpapabuti ng paglaki ng mga ito.[146] Sa Aprika sa mga babaeng buntis at nagpapasuso na may nakompromisong nutrisyon, ang suplementasyon ng multibitamina ay nagpabuti ng mga kalalabasan para sa parehong mga ina at mga sanggol.[146] Ang pag-inom ng mga mikronutriento sa mga lebel ng RDA ng mga matandang tao na nahawaan ng HIV ay nirerekomiyenda ng World Health Organization.[148][149] Karagdagang isinasaad ng WHO na ang suplementasyon ng bitamina A, zinc, at iron sa ilang mga pag-aaral ay maaaring lumikha ng mga epektong adberso sa mga matatandang tao na nahawaan ng HIV.[149] Walang sapat na ebidensiya upang suportahan ang paggamit ng mga medisinang herbal.[150]
Latentong HIV reservoir[baguhin | baguhin ang wikitext]
Sa kabilan ng tagumpay ng mataas na aktibong terapiyang antiretroviral (highly active antiretroviral therapy o HAART) sa pagkokontrol ng impeksiyong HIV at pagbabawas ng kamatayang kaugnay ng HIV, ang mga kasulukuyang rehimeng droga ay walang kakayahan na kompletong malipol ang impeksiyong HIV. Maraming mga taong nasa HAART ay nagkakamit ng pagsupil ng HIV sa mababa sa hangganan ng deteksiyon ng pamantayang mga klinikal na assay para sa maraming mga taon. Gayunpaman, sa paghinto ng HAART, ang bigat viral ng HIV ay mabilis na bumabalik na may sabay na pagbaba ng mga CD4+ na T-Selula na sa karamihan ng mga mga kaso na walang pagbalik sa paggamot ay tumutuloy sa AIDS.
Upang matagumpay na maparami ang sarili nito, ang HIV ay dapat kumomberte ng RNA genome nito sa DNA na nag-aangkat naman sa nucleus ng selula ng hosto (host) at nagpapasok sa genome ng hosto sa pamamagitan ng aksiyon ng HIV integrase. Dahil ang pangunahing selular na inaasinta ng HIV ang CD4+ T-Selula ay gumagampan bilang memoryang mga selula ng sistemang immuno, ang isinamang HIV ay maaaring manataling tulog (dormant) sa loob ng maraming mga taon at posible sa mga dekada. Ang latentong reservoir ay maaaring masukat sa pamamagitan ng kapwa-pagkukultura ng mga CD4+ T-Selula mula sa mga nahawaang pasyente sa mga CD4+ T-Selula mula sa hindi hawaang mga donor at sukatin ang protinang HIV o RNA.
Ang pagkabigo ng mga kandidatong bakuna upang pumrotekta laban sa impeksiyong HIV at pagpapatuloy sa AIDS ay tumungo sa binagong pokus sa mga biolohikal na mekanismong responsable sa latensiya ng HIV. Ang isang limitadong panahon ng terapiya na nagsasama ng mga anti-retroviral sa mga droga na umaasinta ng latentong reservoir ay maaaring sa hinaharap ay pumayag sa kabuuang paglipol ng impeksiyong HIV.
Prognosis[baguhin | baguhin ang wikitext]
Kung walang paggamot, ang net median na panahong ng pagpapatuloy (survival) ng buhay pagkatapos pagkahawa sa HIV ay tinatantiyang mga 9 hanggang 11 mga tao depende sa pangilalim na uri (subtype) na HIV at ang median na rate ng pagpaptuloy pagkatapos ng diagnosis ng AIDS sa mga kapaligirang limitado sa mga mapagkukunan na ang paggamot ay hindi makukuha ay sumasaklaw sa pagitan ng 6 hanggang mga 19 buwan depende sa pag-aaral. Sa mga area, na ang HAART ay malawak na makukuha para sa impeksiyong HIV at AIDS ay nabawasan ang rate ng kamatayan mula sa sakit nito nang mga 80% at nagpataas ng ekspektansiya ng buhay (natitirang inaasahang buhay) para sa mga bagong na-diagnose na impektado ng HIV na indibidwal ay mga 20 hanggang 50 taon.
Habang ang mga bagong paggamot ay patuloy na pinauunlad at dahil ang HIV ay patuloy na nag-eebol ng resistansiya (hindi pagtalab) sa mga gamot, ang pagtatantiya ng panahong ng pagpapatuloy (survival) ay malamang patuloy na magbago. Kung walang terapiyang antiretroviral, ang kamatayan ay normal na nangyayari sa loob ng isang taon pagkatapos na ang indbidwal ay nagpatuloy sa AIDS. Ang karamihan sa mga pasyente ay namamatay mula sa mga oportunistikong mga impeksiyon o mga malignansiyang kaugnay ng patuloy na pagkabigo ng sistemang immuno. Ang rate ng klinikal pagpapatuloy ng sakit ay malawak na nag-iiba sa pagitan ng mga indbidwal at naipakitang apektado ng maraming mga paktor gaya ng suseptibilidad (madaling mahawaan) at pangangalang pangkalusugan ng pagganang immuno at mga kapwa-impeksiyon, gayundin kung aling partikular na strain ng virus ang sangkot.
Epidemiolohiya[baguhin | baguhin ang wikitext]
Tinatantiya ng UNAIDS at WHO (World Health Organization) na ang AIDS ay pumatay ng mahigit 25 milyong mga tao sa pagitan ng 1981 nang ito ay unang makilala at 2005 na gumagawa rito na isa sa pinakadestruktibong pandemika sa itinalang kasaysayan. Sa kabila ng napabuting paglapit (access) sa paggamot antiretroviral at pangangalaga sa maraming mga rehiyon sa buong mundo, ang pandemikang AIDS ay pumatay ng tinatantiyang 2.8 milyon (sa pagitan ng 2.4 at 3.3 milyon) na ang higit sa kalahting milyon (570,000) ay mga bata.
Tinantiya rin ng UNAIDS na ang 33.3 milyong mga tao ay nabubuhay na may HIV sa dulo ng 2009 na tumaas mula 26.2 noong 1999. Kanilang tinantiya ang kaugnay ng AIDS na kamatayan noong 2009 na 1.8 milyon na bumaba sa tuktok (peak) na 2.1 milyon noong 2004 at ang mga bagong impeksiyon na 2.6 milyon na bumaba sa tuktok na 3.2 milyong noong 1997, at ang bilang ng mga indibidwal sa mababa o gitnang sahod (middle income) na mga bansa na tumatanggap ng terapiyang antiretroviral noong 2009 na 5.2 milyon na tumaas mula 4 milyon noong 2008.
Ang Sub-Saharan Africa ay nananatili hanggang ngayon na pinaka masamang apektadong rehiyon na may tinatantiyang 22.5 milyong na kasalukuyang nabubuhay na may HIV (67% ng kabuuang pandaigdig), 1.3 milyong kamatayan (72% ng kabuuang pandaigdig) at 1.8 mga bagong impeksiyon (69% ng kabuuang pandaigdig). Gayunpaman, ang bilang ng mga bagong impeksiyon ay bumaba nang 19% sa buong rehiyong ito mula 2001 at 2009 at nang mahigit mga 25% sa 22 mga bansa sa sub-Saharan Africa sa panahong ito. Ang Asya ang ikalawang pinakamasamang apektadong rehiyon na may 4.9 milyong mga indidbiwal na nabubuhay na may HIV (15% ng kabuuang pandaigdig).
Ang pinakahuling ulat ng pagsusuri ng World Bank's Operations Evaluation Department ay tumataya ng pagiging epektibo ng pagpapaunlad ng World Bank's country-level HIV/AIDS na asistansiya na inilalawan bilang dialogong patakaran, analitikong gawain at pagpapautang na may hayagang layunin ng pagbabawas ng sakop o epekto ng epidemikong AIDS. Ito ang unang komprehensibong pagsusuri ng HIV/AIDS suporta ng World Bank sa mga bansa mula sa pagsisimula ng epedimikang ito hanggang gitnang 2004. Dahil sa ang World Bank ay naglalayong tumulong sa pagpapatupad ng mga pambansang pamahalaang programa, ang kanilang karanasan ay nagbibigay ng mahalagang kabatiran kung paanong ang mga pambansang programa para sa AIDS ay magagawang mas epektibo.
Ang pagpapaunlad ng HAART bilang isang epektibong terapiya ng impeksiyong HIV ay malaking nakabawas ng rate ng kamatayan mula sa sakit na ito sa mga area kung saan ang mga gamot na ito ay malawak na makukuha. Dahil sa ang ekspektansiya ng buhay ng mga indibidwal na may HIV ay dumagdag sa mga bansang ang HAART ay malawak na ginagamit, ang patuloy na pagkalat ng sakit na ito ay nagsanhi ng bilang ng mga taong nabubuhay na may HIV na labis na tumaas.
Sa Aprika, ang bilang ng mga kasong pagpasang HIV ng ina-sa-anak (mother-to-child-transmission o MTCT) at pagiging laganap ng AIDS ang nagsimulang bumaliktad ng mga dekada ng matatag na pagpapatuloy ng buhay sa mga bata. Ang mga bansang gaya ng Uganda ay nagtatangkang supilin ang epidemikang MTCT sa pamamagitan ng pag-aalok ng mga serbisyong VCT (voluntary counselling and testing/boluntaryong pagpapayo at pagsubok), PMTCT (prevention of mother-to-child transmission/pag-iwas na ina-sa-anak na transmisyon) at ANC (ante-natal care/pangangalagang ante-natal) na kinabibilangan ng pamamahagi ng terapiyang antiretroviral.
Kasaysayan[baguhin | baguhin ang wikitext]
Mga pinagmulan[baguhin | baguhin ang wikitext]
Ang HIV ay inakalang nagmula sa hindi-taong mga primado sa sub-Saharan Aprika at naipasa sa mga tao sa huli ng ika-19 o simula ng ika-20 siglo. Ang unang papel na kumikilala ng paterno (pattern) ng mga oportunistikong impeksiyon na katangian ng AIDS ay naiulat noong 1981.
Ang parehong HIV-1 at HIV-2 ay pinaniniwalaang nagmula sa Kanularang-Sentral na Aprika at tumalon sa mga species (isang prosesong tinatawag na zoonosis) mula sa hindi-taong mga primado tungo sa mga tao (humans). Ang HIV-1 ay lumilitaw na nagmula sa katimugang Cameroon sa pamamagitan ng ebolusyon ng SIV (cpz) na isang simiang immunodeficiency virus (SIV) na humahawa ng mga ligaw (wild) na chimpanzee. Ang HIV-1 ay nagmula sa SIVcpz enedemiko sa pangilalim na species/subspecies ng chimpanzee na Pan troglodytes troglodytes. Ang pinakamalapit na kamag-anak ng HIV-2 ang SIV (smmm) na isang virus ng sooty mangabey (Cercocebus atys atys) na isang Lumang Daigdig na unggoy na nabubuhay sa litoral na Kanlurang Aprika mula katimugang Senegal hanggang kanluraning Ivory Coast. Ang mga Lumang Daigdig na mga unggoy gaya ng mga kwagong unggoy ay hindi tinatalaban ng impeksiyong HIV-1 na posibleng dahil sa genomikong fusion ng dalawang gene ng resistansiya (pagiging hindi tinatablan). Ang HIV-1 ay inakalang tumalon sa harang ng species sa hindi bababa sa tatlong magkahiwalay na mga okasyon na nagpalitaw ng tatlong mga pangkat ng virus na M, N, at O.
May ebidensiyang ang mga tao na nakilahok sa mga gawaing bushmeat bilang mga mangangaso (hunters) o tagatinda ng bushmeat ay karaniwang nagtatamo ng SIV. Gayunpaman, ang SIV ay isang mahinang virus. Ito ay karaniwang sinusupil ng sistemang immuno ng tao sa loob ng mga linggo ng pagkakahawa nito. Inakalang ang ilang mga pagpasa ng virus mula indibidwal-sa-indibidwal sa mabilis na paghalili ay kailangan upang pumayag sa sapat na panahong ito ay mag-mutado (mutate) sa HIV. Sa karagdagan, dahil sa relatibong mababang rate ng tao-sa-taong pagpasa nito, ito ay maaari lamang kumalat sa kabuuan ng populasyon sa presensiya ng isa o higit sa mga kanelong (channels) pagpasang mataas na panganib na inakalang hindi umiiral sa Aprika bago ang ika-20 siglo.
Ang spesipikong minungkahing mga kanelong pagpasang mataas na panganib na pumapayag sa virus na maka-angkop (adapt) sa mga tao at kumalat sa buong lipunan ay depende sa iminungkahing panahong ng hayop-sa-taong pagtawid. Ang mga henetikong pag-aaral ng virus ay nagmumungkahing ang pina-kamakailang (most recent) na ninuno ng HIV-1 M pangkat ay pinepetasahan ng pabalik sa circa 1910. Ang mga tagataguyod ng petsang ito ay nag-uugnay ng epidemikang HIV sa paglitaw ng kolonyalismo at paglago ng malaking mga kolonyal na siyudad Aprika na tumungo sa pagbabagong panlipunan kabilang ang mas mataas na digri ng sekswual na promiskuidad, pagkalat ng prostitusyon at ang sabay na mataas na prekwensiyang mga sakit na genital ulcer gaya ng syphilis sa mga bagong kolonyal na siyudad. May ebidensiyang ang mga rate ng transmisyon ng HIV sa pakikipagtalik pampuke bagaman medyo mababa sa ilalim ng mga regular na sirkunstansiya ay maaaring tumaas ng mga sampu kung hind daang beses kung ang isa sa mga katalik ay dumadanas ng Sakit na naipapasa sa pakikipagtalik (STD) na resulta ng genital ulcer. Ang simula nang 1900 na mga kolonyal na mga siyudad ay kilala dahil sa mataas na paglaganap ng prostitusyon at STD na genital ulcer sa digri na noong 1928, kasingrami ng 45% ng mga residenteng babae ng silanganing Kinshasa ay inakalang mga prostitut at noong 1933, ang mga 15% ng lahat ng mga resident ng parehong siyudad ay impektado ng isa sa mga anyo ng syphilis.
Ang alternatibong pananaw ay nagsasaad na ang hindi ligtas na mga kasanayang medikal sa Aprika sa mga panahong pagkatapos ng Ikalawang Digmaang Pandaigdig gaya ng hindi sterilisadong muling paggamit pang-isahing gamit na mga siringhe (syrigne) habang isinasagawa ang pangmasang pagbabakuna, mga kampanyang paggamot na antibiotiko at anti-malaria ang inisyal na mga vector na pumayag sa virus na maka-angkop (adapt) sa mga tao at kumalat.
Ang pinakaunang maiging nadokumentong kaso ng HIV sa tao ay pinetsahan ng pabalik sa 1959. Ang virus na HIV ay maaaring umiiral na sa Estados Unidos sa simula ng 1966 ngunit ang malawak na karamihang mga impeksiyon ay nangyayari sa labas ng Sub-Saharan Aprika (kabilang ang Estados Unidos) ay mababakas pabalik sa isang hindi kilalang indibidwal na nahawaan ng HIV sa Haiti at nagdala naman ng impeksiyon sa Estados Unidos noong mga 1969. Ang epidemika ay mabilis namang kumalat sa mga mataas na panganib na pangkat (sa simula ay mga seksuwal na promiskuosong mga homoseksuwal). Noong 1978, ang pagiging laganap ng HIV-1 sa mga baklang lalakeng resident ng New York at San Francisco ay tinatantiyang 5% na nagmumungkahing ang ilang mga libong indibidwal sa Estados Unidos ay nahawaan na sa panahong ito.
Pagkakatuklas[baguhin | baguhin ang wikitext]
Ang AIDS ay unang klinikal na napagmasdan sa pagitan ng huli nang 1980 at simula nang 1981. Ang mga tagagamit ng panturok ng droga (drug injection) at mga homoseksuwal na lalakeng hindi alam ang dahilan ng huminang immunidad ay nagpakita ng mga sintomas ng Pneumocystis carinii pneumonia (PCP) na isang bihirang oportunistikong impeksiyon na alam sa mga panahong ito na nakikita sa mga taong may labis na nakomopromisong (huminang) mga sistema ng immuno. Sandaling pagkatapos nito, ang karagdagang mga baklang lalake ay nakitaan ng nakaraang bihirang kanser ng balat na tinatawag na Kaposi’s sarcoma (KS). Marami pang mga kaso ng PCP at KS ang mabilis na lumitaw na umalerto sa Centers for Disease Control and Prevention (CDC) ng Estados Unidos. Ang isang CDC task force ay binuo upang imonitor ang pagsiklab ng mga kasong ito. Pagkatapos makilala ang isang paterno ng anomalosong mga sintomas na nakikita sa mga pasyente, pinangalan ng CDC task force ang kondisyong ito na acquired immune deficiency syndrome (AIDS).
Noong 1983, ang dalawang magkahilaway na mga pangkat pagsasaliksik na pinangunahan nina Robert Gallo at Luc Montagnier ay independiyenteng naghayag na ang isang nobelang (novel) retrovirus ay maaaring umaapekto sa mga pasyente ng AIDS at kanilang inilimbang ang kanilang mga natuklasan sa parehong isyu ng hornal na Science. Inangkin ni Gallo na ang virus na naihiwalay (isolated) ng kanyang pangkat mula sa pasyente ng AIDS ay mapapansing katulad sa hugis sa ibang pantaong T-lymphotropic viruses (HTLVs) na ang kanyang pangkat ang unang naghiwalay. Tinawag ng pangkat ni Gallo ang kanilang bagong naihiwalay na virus na HTLV-III. Sa parehong panahon, ang pangkat ni Montagneir ay naghiwalay ng virus mula sa pasyenteng kinakikitaan ng lymphadenopatiya (pamamaga ng kulani) ng leeg at kahinaang pisikal na dalawang mga klasikong sintomas ng AIDS. Sa pagsasalungat ng ulat mula sa pangkat ni Gallo, si Montagnier at ang kanyang mga kasama ay nagpakitang ang core na mga protina ng virus na ito ay immunolohikal na iba mula sa nasa HTLV-I. Pinangalan ng pangkat ni Montagnier ang kanilang naihiwalay na virus na lymphadenopathy-associated virus (LAV). Ang pangalang HIV ay napili bilang kompromiso sa pagitan ng mga dalawang pang-aankin na LAV at HTLV-III.
Kung si Gallo o Montagnier ang nararapat ng mas higit na kredito sa pagkakatuklas ng virus na nagsasanhi ng AIDS ay isang bagay ng malaking kontrobersiya. Kasama ng kanyang kasamang si Françoise Barré-Sinoussi, si Montagnier ay ginawaran ng kalahati ng 2008 Gantimpalang Nobel sa Physiolohiya o Medisina sa kanyang "pagkakatuklas ng human immunodeficiency virus". Si Harald zur Hausen ay nakisalo rin sa Gantimpalang Nobel sa kanyang pagkakatuklas na ang human papilloma virus ay tumutungo sa kanser na serbikal ngunit si Gallo ay hindi isinama. Sinabi ni Gallo na "isang pagkasiphayo" na hindi siya napangalanan bilang kapwa resipyente ng Gantimpalang Nobel. Sinabi ni Montagnier na siya ay "nagulat" na si Gallo ay hindi kinilala ng komite ng Nobel na sinasabing: "Mahalaga sa akin na mapatunayang ang HIV ang sanhi ng AIDS at si Gallo ay may napakahalagang papel dito. Ako'y labis na nalulungkot para kay Robert Gallo."
Pagtanggi sa AIDS[baguhin | baguhin ang wikitext]
Ang maliit na pangkat ng mga indibidwal ay patuloy na tumututol sa koneksiyon sa pagitan ng HIV at AIDS, pagtanggi sa pag-iral ng mismong HIV o ang balidad ng pagsubok (testing) ng HIV at mga paraang paggamot. Ang mga pag-aangking ito na tinatawag na AIDS denialism ay sinuri at itinakwil ng pamayanang siyentipiko. Gayunpaman, ang mga pangkat na ito ay may malaking epektong pampolitika partikular na sa Timog Aprika kung saan ang opisyal na pagyakap ng pamahaalan nito sa AIDS denialism ay responsable sa hindi epektibo nitong tugon sa epidemikang AIDS sa bansang ito at sinisi sa daang mga libong maiiwasang kamatayan at mga impeksiyong HIV.
Pananaliksik[baguhin | baguhin ang wikitext]
Transplantasyon ng stem cell[baguhin | baguhin ang wikitext]
Noong 2007, ang isang 40 taong gulang lalakeng positibo sa HIV ay nabigyan ng stem cell transplant bilang bahagi ng kanyang paggamot para sa acute myelogenous leukemia (AML). Ang ikalawang transplant ay isinagawa pagkatapos ng isang taon pagkatapos ng relapse (pagbalik sa dating kondisyon). Ang donor ay napili hindi laman dahil sa kompatibilidad henetiko kundi dahil sa pagiging homozygous rin para sa mutasyong CCR5-Δ32 na nagbibigay ng resistansiya (pagiging hindi tinatablan) sa impeksiyong HIV. Pagkatapos ng 20 buwan na walang paggamot ng drogang antiretroviral, iniulat na ang mga lebel ng HIV sa dugo ng tumanggap nito, marrow ng buto at bower ay mababa sa hangganan (limit) ng deteksiyon. Ang virus ay nanatiling hindi matukoy (undetectable) sa paglipas ng tatlong taon pagakatapos ng unang transplant. Bagaman inilarawan ng mga mananaliksik at komentador ang resultang ito bilang lunas (cure) ang iba ay nagmungkahing ang virus ay maaaring nananatiling tago sa mga tisyu gaya ng utak na isang viral reservoir. Ang paggamot gamit ang stem cell ay nananatiling iniimbestigahan dahil sa kalikasang anekdotal nito, ang sakit at ang panganib ng kamatayan na kaugnay ng mga stem cell transplant at ang kahirapan ng paghanap ng mga angkop na donor ng stem cell.
Mga ahenteng immunomodulatoryo[baguhin | baguhin ang wikitext]
Sa pagkokomplementa ng mga pagsisikap na kontrolin ang replikasyon ng virus, ang mga immunoterapiya na maaaring makatulong sa paggaling ng sistemang immuno ay siniyasat sa nakaraan at may mga patuloy na pagsubok (trial) na isinasagawa kabilang ang IL-2 at IL-7.
Sanggunian[baguhin | baguhin ang wikitext]
- ↑ Sepkowitz KA (2001). "AIDS—the first 20 years". N. Engl. J. Med. 344 (23): 1764–72. doi:10.1056/NEJM200106073442306. PMID 11396444.
{{cite journal}}: Unknown parameter|month=ignored (tulong) - ↑ Markowitz, edited by William N. Rom ; associate editor, Steven B. (2007). Environmental and occupational medicine (4th pat.). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. p. 745. ISBN 978-0-7817-6299-1.
{{cite book}}:|first=has generic name (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ "HIV and Its Transmission". Centers for Disease Control and Prevention. 2003. Inarkibo mula sa orihinal noong 2005-02-04. Nakuha noong 23 Mayo 2006.
- ↑ Sharp, PM; Hahn, BH (2011 Sep). "Origins of HIV and the AIDS Pandemic". Cold Spring Harbor perspectives in medicine. 1 (1): a006841. doi:10.1101/cshperspect.a006841. PMC 3234451. PMID 22229120.
{{cite journal}}: Check date values in:|date=(tulong) - ↑ Gallo RC (2006). "A reflection on HIV/AIDS research after 25 years". Retrovirology. 3: 72. doi:10.1186/1742-4690-3-72. PMC 1629027. PMID 17054781.
- ↑ "Global Report Fact Sheet" (PDF). UNAIDS. 2010. Inarkibo mula sa ang orihinal (PDF) noong 2013-03-19. Nakuha noong 2012-08-18.
- ↑ 7.0 7.1 7.2 UNAIDS 2011 pg. 1–10
- ↑ Kallings LO (2008). "The first postmodern pandemic: 25 years of HIV/AIDS". J Intern Med. 263 (3): 218–43. doi:10.1111/j.1365-2796.2007.01910.x. PMID 18205765. (subscription required)
- ↑ International Committee on Taxonomy of Viruses (2002). "61.0.6. Lentivirus". National Institutes of Health. Nakuha noong 2006-02-28.
- ↑ International Committee on Taxonomy of Viruses (2002). "61. Retroviridae". National Institutes of Health. Nakuha noong 2006-02-28.
- ↑ Lévy, J. A. (1993). "HIV pathogenesis and long-term survival". AIDS. 7 (11): 1401–10. doi:10.1097/00002030-199311000-00001. PMID 8280406.
- ↑ Smith, Johanna A.; Daniel, René (Division of Infectious Diseases, Center for Human Virology, Thomas Jefferson University, Philadelphia) (2006). "Following the path of the virus: the exploitation of host DNA repair mechanisms by retroviruses". ACS Chem Biol. 1 (4): 217–26. doi:10.1021/cb600131q. PMID 17163676.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Gilbert, PB; McKeague, IW; Eisen, G; Mullins, C; Guéye-Ndiaye, A; Mboup, S; Kanki, PJ; et al. (28 Pebrero 2003). "Comparison of HIV-1 and HIV-2 infectivity from a prospective cohort study in Senegal". Statistics in Medicine. 22 (4): 573–593. doi:10.1002/sim.1342. PMID 12590415.
{{cite journal}}: Explicit use of et al. in:|first=(tulong) - ↑ Reeves, J. D. and Doms, R. W (2002). "Human Immunodeficiency Virus Type 2". J. Gen. Virol. 83 (Pt 6): 1253–65. doi:10.1099/vir.0.18253-0. PMID 12029140.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Grabar, S., Selinger-Leneman, H., Abgrall, S., Pialoux, G., Weiss, L., Costagliola, D. (2009). "Prevalence and comparative characteristics of long-term nonprogressors and HIV controller patients in the French Hospital Database on HIV". AIDS. 23 (9): 1163–1169. doi:10.1097/QAD.0b013e32832b44c8. PMID 19444075.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Blankson, JN (2010 Mar). "Control of HIV-1 replication in elite suppressors". Discovery medicine. 9 (46): 261–6. PMID 20350494.
{{cite journal}}: Check date values in:|date=(tulong) - ↑ Piatak, M., Jr, Saag, M. S., Yang, L. C., Clark, S. J., Kappes, J. C., Luk, K. C., Hahn, B. H., Shaw, G. M. and Lifson, J.D. (1993). "High levels of HIV-1 in plasma during all stages of infection determined by competitive PCR". Science. 259 (5102): 1749–1754. Bibcode:1993Sci...259.1749P. doi:10.1126/science.8096089. PMID 8096089.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Pantaleo G, Demarest JF, Schacker T, Vaccarezza M, Cohen OJ, Daucher M, Graziosi C, Schnittman SS, Quinn TC, Shaw GM, Perrin L, Tambussi G, Lazzarin A, Sekaly RP, Soudeyns H, Corey L, Fauci AS. (1997). "The qualitative nature of the primary immune response to HIV infection is a prognosticator of disease progression independent of the initial level of plasma viremia". Proc Natl Acad Sci U S A. 94 (1): 254–258. Bibcode:1997PNAS...94..254P. doi:10.1073/pnas.94.1.254. PMC 19306. PMID 8990195.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Kahn, J. O. and Walker, B. D. (1998). "Acute Human Immunodeficiency Virus type 1 infection". N. Engl. J. Med. 331 (1): 33–39. doi:10.1056/NEJM199807023390107. PMID 9647878.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Daar ES, Little S, Pitt J; et al. (2001). "Diagnosis of primary HIV-1 infection. Los Angeles County Primary HIV Infection Recruitment Network". Ann. Intern. Med. 134 (1): 25–9. PMID 11187417.
{{cite journal}}: Explicit use of et al. in:|author=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑
Burton GF, Keele BF, Estes JD, Thacker TC, Gartner S. (2002). "Follicular dendritic cell contributions to HIV pathogenesis". Semin Immunol. 14 (4): 275–284. doi:10.1016/S1044-5323(02)00060-X. PMID 12163303.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Clapham PR, McKnight A. (2001). "HIV-1 receptors and cell tropism". Br Med Bull. 58 (4): 43–59. doi:10.1093/bmb/58.1.43. PMID 11714623.
- ↑ Smith DK, Grohskopf LA, Black RJ; et al. (2005). "Antiretroviral postexposure prophylaxis after sexual, injection-drug use, or other nonoccupational exposure to HIV in the United States: recommendations from the U.S. Department of Health and Human Services". MMWR Recomm Rep. 54 (RR–2): 1–20. PMID 15660015. Nakuha noong 2009-03-31.
{{cite journal}}: Explicit use of et al. in:|author=(tulong); Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ 24.0 24.1 24.2 24.3 Jin F; et al. (2010). "Per-contact probability of HIV transmission in homosexual men in Sydney in the era of HAART". AIDS. 24 (6): 907–913. doi:10.1097/QAD.0b013e3283372d90. PMC 2852627. PMID 20139750.
{{cite journal}}: Explicit use of et al. in:|author=(tulong); Unknown parameter|month=ignored (tulong) - ↑ Donegan E, Stuart M, Niland JC; et al. (1990). "Infection with human immunodeficiency virus type 1 (HIV-1) among recipients of antibody-positive blood donations". Ann. Intern. Med. 113 (10): 733–739. PMID 2240875.
{{cite journal}}: Explicit use of et al. in:|author=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ 26.0 26.1 26.2 26.3 Coovadia H (2004). "Antiretroviral agents—how best to protect infants from HIV and save their mothers from AIDS". N. Engl. J. Med. 351 (3): 289–292. doi:10.1056/NEJMe048128. PMID 15247337.
- ↑ Kaplan EH, Heimer R (1995). "HIV incidence among New Haven needle exchange participants: updated estimates from syringe tracking and testing data". J. Acquir. Immune Defic. Syndr. Hum. Retrovirol. 10 (2): 175–176. PMID 7552482.
- ↑ Bell DM (1997). "Occupational risk of human immunodeficiency virus infection in healthcare workers: an overview". Am. J. Med. 102 (5B): 9–15. doi:10.1016/S0002-9343(97)89441-7. PMID 9845490.
- ↑ 29.0 29.1 29.2 29.3 29.4 29.5 Boily MC, Baggaley RF, Wang L, Masse B, White RG, Hayes RJ, Alary M (2009). "Heterosexual risk of HIV-1 infection per sexual act: systematic review and meta-analysis of observational studies". The Lancet Infectious Diseases. 9 (2): 118–129. doi:10.1016/S1473-3099(09)70021-0. PMID 19179227.
{{cite journal}}: Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ 30.0 30.1 30.2 30.3 European Study Group on Heterosexual Transmission of HIV (1992). "Comparison of female to male and male to female transmission of HIV in 563 stable couples. European Study Group on Heterosexual Transmission of HIV". BMJ. 304 (6830): 809–813. doi:10.1136/bmj.304.6830.809. PMC 1881672. PMID 1392708.
- ↑ 31.0 31.1 31.2 31.3 31.4 31.5 Varghese B, Maher JE, Peterman TA, Branson BM,Steketee RW (2002). "Reducing the risk of sexual HIV transmission: quantifying the per-act risk for HIV on the basis of choice of partner, sex act, and condom use". Sex. Transm. Dis. 29 (1): 38–43. doi:10.1097/00007435-200201000-00007. PMID 11773877.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Leynaert B, Downs AM, de Vincenzi I (1998). "Heterosexual transmission of human immunodeficiency virus: variability of infectivity throughout the course of infection. European Study Group on Heterosexual Transmission of HIV". Am. J. Epidemiol. 148 (1): 88–96. PMID 9663408.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ 33.0 33.1 Millett GA, Flores SA, Marks G, Reed JB, Herbst JH (2009). "Circumcision status and risk of HIV and sexually transmitted infections among men who have sex with men: a meta-analysis". The Journal of American Medical Association. 300 (14): 1674–1684. doi:10.1001/jama.300.14.1674. PMID 18840841. Nakuha noong 2010-04-11.
{{cite journal}}: Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Correction about the values although "the pattern of nonsignificant findings remains consistent with the originally published article"[1] Naka-arkibo 2007-05-15 sa Wayback Machine.
- ↑ "Public Health Agency of Canada". Phac-aspc.gc.ca. 2004-12-01. Inarkibo mula sa ang orihinal noong 2012-06-23. Nakuha noong 2010-07-28.
- ↑ "University of Hartford". uhavax.hartford.edu/. 2002-03-19. Inarkibo mula sa ang orihinal noong 2011-09-30. Nakuha noong 2011-08-14.
- ↑ National Institute of Allergy and Infectious Diseases (2001-07-20). Workshop Summary: Scientific Evidence on Condom Effectiveness for Sexually Transmitted Disease (STD) Prevention (PDF). Hyatt Dulles Airport, Herndon, Virginia. pp. 13–15. Inarkibo mula sa ang orihinal (PDF) noong 2010-03-15. Nakuha noong 2009-01-08.
{{cite conference}}: Unknown parameter|coauthors=ignored (|author=suggested) (tulong) - ↑ "Should spermicides be used with condoms?". Condoms and Sexually Transmitted Diseases, Brochure. United States Food and Drug Administration. 2009-04-30. Inarkibo mula sa ang orihinal noong 2013-02-13. Nakuha noong 2009-07-23.
- ↑ Global Campaign for Microbicides : Rectal Use of N-9 Naka-arkibo 2012-08-21 sa Wayback Machine. checked 2009-07-22
- ↑ Nonoxynol-9 Spermicide on HIV Risk List Naka-arkibo 2012-08-21 sa Wayback Machine. checked 2009-07-22
- ↑ Williams BG, Lloyd-Smith JO, Gouws E, Hankins C, Getz WM, Hargrove J, de Zoysa I, Dye C, Auvert B. (2006). "The Potential Impact of Male Circumcision on HIV in Sub-Saharan Africa". PLoS Med. 3 (7): e262. doi:10.1371/journal.pmed.0030262. PMC 1489185. PMID 16822094.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Bailey RC, Moses S, Parker CB; et al. (2007). "Male circumcision for HIV prevention in young men in Kisumu, Kenya: a randomised controlled trial". Lancet. 369 (9562): 643–56. doi:10.1016/S0140-6736(07)60312-2. PMID 17321310.
{{cite journal}}: Explicit use of et al. in:|author=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Gray RH; et al. (24 Pebrero 2007). "Male circumcision for HIV prevention in men in Rakai, Uganda: a randomised trial". Lancet. 369 (9562): 657–66. doi:10.1016/S0140-6736(07)60313-4. PMID 17321311.
{{cite journal}}: Cite has empty unknown parameter:|quotes=(tulong); Explicit use of et al. in:|author=(tulong) - ↑ WHO (2007). "WHO and UNAIDS announce recommendations from expert consultation on male circumcision for HIV prevention". WHO.int. Inarkibo mula sa ang orihinal noong 2013-03-12. Nakuha noong 2007-07-13.
- ↑ Maslovskaya O, Brown JJ, Padmadas SS (2009). "Disentangling the complex association between female genital cutting and HIV among Kenyan women". J Biosoc Sci. 41 (6): 815–30. doi:10.1017/S0021932009990150. PMID 19607733.
{{cite journal}}: Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Utz-Billing I, Kentenich H (2008). "Female genital mutilation: an injury, physical and mental harm". J Psychosom Obstet Gynaecol. 29 (4): 225–9. doi:10.1080/01674820802547087. PMID 19065392.
{{cite journal}}: Unknown parameter|month=ignored (tulong) - ↑ Nyindo M (2005). "Complementary factors contributing to the rapid spread of HIV-I in sub-Saharan Africa: a review". East Afr Med J. 82 (1): 40–6. PMID 16122111.
{{cite journal}}: Unknown parameter|month=ignored (tulong) - ↑ Mboto CI, Fielder M, Davies-Russell A, Jewell AP (2009). "Prevalence of HIV-1, HIV-2, hepatitis C and co-infection in The Gambia". West Afr J Med. 28 (1): 16–9. PMID 19662739.
{{cite journal}}: Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Underhill K, Operario D, Montgomery P (2008). Operario, Don (pat.). "Abstinence-only programs for HIV infection prevention in high-income countries". Cochrane Database of Systematic Reviews (4): CD005421. doi:10.1002/14651858.CD005421.pub2. PMID 17943855.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Lifson AR (1988). "Do alternate modes for transmission of human immunodeficiency virus exist? A review". JAMA. 259 (9): 1353–6. doi:10.1001/jama.259.9.1353. PMID 2963151.
- ↑ "Why Mosquitoes Cannot Transmit AIDS [HIV virus]". Rci.rutgers.edu. Inarkibo mula sa ang orihinal noong 2014-03-29. Nakuha noong 2010-07-28.
- ↑ Cochrane Systematic Review on interventions for prevention of late postnatal mother-to-child transmission of HIV http://www.cochrane.org/reviews/en/ab006734.html
- ↑ UNAIDS. "2009 AIDS Epidemic Update" (PDF). Nakuha noong 2010-10-24
{{cite web}}: CS1 maint: postscript (link) - ↑ Smith D, Richman D, Little S (2005). "HIV Superinfection". Journal of Infectious Diseases. 192 (3): 438–44. doi:10.1086/431682. PMID 15995957.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Gottlieb; Nickle, DC; Jensen, MA; Wong, KG; Grobler, J; Li, F; Liu, SL; Rademeyer, C; Learn, GH; et al. (2004). "Dual HIV-1 infection associated with rapid disease progression". Lancet. 363 (9049): 619–22. doi:10.1016/S0140-6736(04)15596-7. PMID 14987889.
{{cite journal}}: Explicit use of et al. in:|author=(tulong) - ↑ Smith; Wong, JK; Hightower, GK; Ignacio, CC; Koelsch, KK; Daar, ES; Richman, DD; Little, SJ; et al. (2004). "Incidence of HIV superinfection following primary infection". JAMA. 292 (10): 1177–8. doi:10.1001/jama.292.10.1177. PMID 15353529.
{{cite journal}}: Explicit use of et al. in:|author=(tulong) - ↑ Chohan B, Lavreys L, Rainwater SM, Overbaugh J (2005). "Evidence for Frequent Reinfection with Human Immunodeficiency Virus Type 1 of a Different Subtype". J. Virol. 79 (16): 10701–8. doi:10.1128/JVI.79.16.10701-10708.2005. PMC 1182664. PMID 16051862.
{{cite journal}}: Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Piantadosi A, Chohan B, Chohan V, McClelland RS, Overbaugh J (2007). "Chronic HIV-1 Infection Frequently Fails to Protect against Superinfection". PLoS Pathog. 3 (11): e177. doi:10.1371/journal.ppat.0030177. PMC 2077901. PMID 18020705.
{{cite journal}}: Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Hu DJ, Subbarao S, Vanichseni S; et al. (2005). "Frequency of HIV-1 dual subtype infections, including intersubtype superinfections, among injection drug users in Bangkok, Thailand". AIDS. 19 (3): 303–8. PMID 15718841. Inarkibo mula sa ang orihinal noong 2013-09-16. Nakuha noong 2009-03-31.
{{cite journal}}: Explicit use of et al. in:|author=(tulong); Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Fan, H., Conner, R. F. and Villarreal, L. P. eds, pat. (2005). AIDS : science and society (4th pat.). Boston, MA: Jones and Bartlett Publishers. ISBN 0-7637-0086-X.
{{cite book}}:|editor=has generic name (tulong); Cite has empty unknown parameter:|chapterurl=(tulong)CS1 maint: multiple names: mga patnugot (link) - ↑ Karim, Q. A., Karim, S. S. A., Frolich, J. A., Grobler, A. C., Baxter, C., Mansoor, L. E., Kharsany, A. B. M., Sibeko, S., Mlisana, K. P., Omar, Z., Gengiah, T. N., Maarschalk, S., Arulappan, N., Mlotshwa, M., Morris, L., and Taylor, D. (19 Hulyo 2010). "Effectiveness and Safety of Tenofovir Gel, an Antiretroviral Microbicide, for the Prevention of HIV Infection in Women". Science. 329 (5996): 1168–74. Bibcode:2010Sci...329.1168A. doi:10.1126/science.1193748. PMC 3001187. PMID 20643915.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ National Institute of Allergy and Infectious Diseases (NIAID), "Treating HIV-infected People with Antiretrovirals Protects Partners from Infection", NIH News, 2011 May
- ↑ Tolle, MA; Schwarzwald, HL (2010 Hulyo 15). "Postexposure prophylaxis against human immunodeficiency virus". American family physician. 82 (2): 161–6. PMID 20642270.
{{cite journal}}: Check date values in:|date=(tulong) - ↑ Los Alamos National Laboratory • Established 1943. "Fighting the world's most dangerous disease::Los Alamos Lab". Lanl.gov. Inarkibo mula sa ang orihinal noong 2010-12-03. Nakuha noong 2010-07-28.
- ↑ Robb ML (2008). "Failure of the Merck HIV vaccine: an uncertain step forward". Lancet. 372 (9653): 1857–1858. doi:10.1016/S0140-6736(08)61593-7. PMID 19012958.
- ↑ Gray GE, Allen M, Moodie Z; et al. (2011). "Safety and efficacy of the HVTN 503/Phambili Study of a clade-B-based HIV-1 vaccine in South Africa: a double-blind, randomised, placebo-controlled test-of-concept phase 2b study". Lancet Infect Dis. 11 (7): 507–515. doi:10.1016/S1473-3099(11)70098-6. PMID 21570355.
{{cite journal}}: Explicit use of et al. in:|author=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ "HIV vaccine 'reduces infection'". BBC News. 24 Setyembre 2009. Nakuha noong 30 Marso 2010.
- ↑ The Lancet (2009). "A (prime) boost for HIV vaccine research?". Lancet. 374 (9696): 1119. doi:10.1016/S0140-6736(09)61720-7.
- ↑ U.S. Army Office of the Surgeon General (21 Marso 2011). "HIV Vaccine Trial in Thai Adults". ClinicalTrials.gov. Nakuha noong 28 Hunyo 2011.
- ↑ U.S. Army Office of the Surgeon General (2 Hunyo 2010). "Follow up of Thai Adult Volunteers With Breakthrough HIV Infection After Participation in a Preventive HIV Vaccine Trial". ClinicalTrials.gov.
- ↑ McGovern SL, Caselli E, Grigorieff N, Shoichet BK (2002). "A common mechanism underlying promiscuous inhibitors from virtual and high-throughput screening". J Med Chem. 45 (8): 1712–22. doi:10.1021/jm010533y. PMID 11931626.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Compared with overview in: Fisher, Bruce; Harvey, Richard P.; Champe, Pamela C. (2007). Lippincott's Illustrated Reviews: Microbiology (Lippincott's Illustrated Reviews Series). Hagerstown, MD: Lippincott Williams & Wilkins. ISBN 0-7817-8215-5.
{{cite book}}: CS1 maint: multiple names: mga may-akda (link) Page 3 - ↑ 73.0 73.1 73.2 73.3 73.4 73.5 73.6 Various (2008). HIV Sequence Compendium 2008 Introduction (PDF). Nakuha noong 2009-03-31.
- ↑ 74.0 74.1 74.2 Chan, DC., Fass, D., Berger, JM., Kim, PS. (1997). "Core Structure of gp41 from the HIV Envelope Glycoprotein" (PDF). Cell. 89 (2): 263–73. doi:10.1016/S0092-8674(00)80205-6. PMID 9108481. Nakuha noong 2009-03-31.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ National Institute of Health (17 Hunyo 1998). "Crystal Structure of Key HIV Protein Reveals New Prevention, Treatment Targets". Inarkibo mula sa orihinal noong 2006-02-19. Nakuha noong 2006-09-14.
- ↑ Ouellet DL, Plante I, Landry P; et al. (2008). "Identification of functional microRNAs released through asymmetrical processing of HIV-1 TAR element". Nucleic Acids Res. 36 (7): 2353–65. doi:10.1093/nar/gkn076. PMC 2367715. PMID 18299284.
{{cite journal}}: Explicit use of et al. in:|author=(tulong); Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Klase Z, Winograd R, Davis J; et al. (2009). "HIV-1 TAR miRNA protects against apoptosis by altering cellular gene expression". Retrovirology. 6 (1): 18. doi:10.1186/1742-4690-6-18. PMC 2654423. PMID 19220914.
{{cite journal}}: Explicit use of et al. in:|author=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Garcia JV, Miller AD (1991). "Serine phosphorylation-independent downregulation of cell-surface CD4 by nef". Nature. 350 (6318): 508–11. Bibcode:1991Natur.350..508G. doi:10.1038/350508a0. PMID 2014052.
{{cite journal}}: Unknown parameter|month=ignored (tulong) - ↑ Schwartz O, Maréchal V, Le Gall S, Lemonnier F, Heard JM (1996). "Endocytosis of major histocompatibility complex class I molecules is induced by the HIV-1 Nef protein". Nat. Med. 2 (3): 338–42. doi:10.1038/nm0396-338. PMID 8612235.
{{cite journal}}: Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Stumptner-Cuvelette P, Morchoisne S, Dugast M; et al. (2001). "HIV-1 Nef impairs MHC class II antigen presentation and surface expression". Proc. Natl. Acad. Sci. U.S.A. 98 (21): 12144–9. Bibcode:2001PNAS...9812144S. doi:10.1073/pnas.221256498. PMC 59782. PMID 11593029.
{{cite journal}}: Explicit use of et al. in:|author=(tulong); Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ 81.0 81.1 Coakley, E., Petropoulos, C. J. and Whitcomb, J. M. (2005). "Assessing ch vbgemokine co-receptor usage in HIV". Curr. Opin. Infect. Dis. 18 (1): 9–15. doi:10.1097/00001432-200502000-00003. PMID 15647694.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Knight, S. C., Macatonia, S. E. and Patterson, S. (1990). "HIV I infection of dendritic cells". Int. Rev. Immunol. 6 (2–3): 163–75. doi:10.3109/08830189009056627. PMID 2152500.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Tang, J. and Kaslow, R. A. (2003). "The impact of host genetics on HIV infection and disease progression in the era of highly active antiretroviral therapy". AIDS. 17 (Suppl 4): S51–S60. doi:10.1097/00002030-200317004-00006. PMID 15080180.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Zhu T, Mo H, Wang N, Nam DS, Cao Y, Koup RA, Ho DD. (1993). "Genotypic and phenotypic characterization of HIV-1 patients with primary infection". Science. 261 (5125): 1179–81. Bibcode:1993Sci...261.1179Z. doi:10.1126/science.8356453. PMID 8356453.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
van’t Wout AB, Kootstra NA, Mulder-Kampinga GA, Albrecht-van Lent N, Scherpbier HJ, Veenstra J, Boer K, Coutinho RA, Miedema F, Schuitemaker H. (1994). "Macrophage-tropic variants initiate human immunodeficiency virus type 1 infection after sexual, parenteral, and vertical transmission". J Clin Invest. 94 (5): 2060–7. doi:10.1172/JCI117560. PMC 294642. PMID 7962552.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Zhu T, Wang N, Carr A, Nam DS, Moor-Jankowski R, Cooper DA, Ho DD. (1996). "Genetic characterization of human immunodeficiency virus type 1 in blood and genital secretions: evidence for viral compartmentalization and selection during sexual transmission". J Virol. 70 (5): 3098–107. PMC 190172. PMID 8627789.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Muciaccia B, Padula F, Vicini E, Gandini L, Lenzi A, Stefanini M. (2005). "Beta-chemokine receptors 5 and 3 are expressed on the head region of human spermatozoon". FASEB J. 19 (14): 2048–50. doi:10.1096/fj.05-3962fje. PMID 16174786.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Berlier W, Bourlet T, Lawrence P, Hamzeh H, Lambert C, Genin C, Verrier B, Dieu-Nosjean MC, Pozzetto B, Delezay O. (2005). "Selective sequestration of X4 isolates by human genital epithelial cells: Implication for virus tropism selection process during sexual transmission of HIV". J Med Virol. 77 (4): 465–74. doi:10.1002/jmv.20478. PMID 16254974.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Clevestig P, Maljkovic I, Casper C, Carlenor E, Lindgren S, Naver L, Bohlin AB, Fenyo EM, Leitner T, Ehrnst A. (2005). "The X4 phenotype of HIV type 1 evolves from R5 in two children of mothers, carrying X4, and is not linked to transmission". AIDS Res Hum Retroviruses. 5 (21): 371–8. doi:10.1089/aid.2005.21.371. PMID 15929699.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Moore JP. (1997). "Coreceptors: implications for HIV pathogenesis and therapy". Science. 276 (5309): 51–2. doi:10.1126/science.276.5309.51. PMID 9122710.
- ↑
Karlsson A, Parsmyr K, Aperia K, Sandstrom E, Fenyo EM, Albert J. (1994). "MT-2 cell tropism of human immunodeficiency virus type 1 isolates as a marker for response to treatment and development of drug resistance". J Infect Dis. 170 (6): 1367–75. doi:10.1093/infdis/170.6.1367. PMID 7995974.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Koot M, van 't Wout AB, Kootstra NA, de Goede RE, Tersmette M, Schuitemaker H. (1996). "Relation between changes in cellular load, evolution of viral phenotype, and the clonal composition of virus populations in the course of human immunodeficiency virus type 1 infection". J Infect Dis. 173 (2): 349–54. doi:10.1093/infdis/173.2.349. PMID 8568295.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Cheney, K and McKnight, A (2010). "HIV-2 Tropism and Disease". Lentiviruses and Macrophages: Molecular and Cellular Interactions. Caister Academic Press. ISBN 978-1-904455-60-8.
{{cite book}}: CS1 maint: multiple names: mga may-akda (link) - ↑ 94.0 94.1 94.2 94.3 94.4 94.5 94.6 Chan D, Kim P (1998). "HIV entry and its inhibition". Cell. 93 (5): 681–4. doi:10.1016/S0092-8674(00)81430-0. PMID 9630213.
- ↑ 95.0 95.1 95.2 95.3 95.4 95.5 Wyatt R, Sodroski J (1998). "The HIV-1 envelope glycoproteins: fusogens, antigens, and immunogens". Science. 280 (5371): 1884–8. Bibcode:1998Sci...280.1884W. doi:10.1126/science.280.5371.1884. PMID 9632381.
- ↑ Arthos J, Cicala C, Martinelli E, Macleod K, Van Ryk D, Wei D, Xiao Z, Veenstra TD, Conrad TP, Lempicki RA, McLaughlin S, Pascuccio M, Gopaul R, McNally J, Cruz CC, Censoplano N, Chung E, Reitano KN, Kottilil S, Goode DJ, Fauci AS. (2008). "HIV-1 envelope protein binds to and signals through integrin alpha (4)beta (7), the gut mucosal homing receptor for peripheral T cells". Nature Immunol. In Press (3): 301. doi:10.1038/ni1566. PMID 18264102.
{{cite journal}}: More than one of|pages=at|page=specified (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ 97.0 97.1 Pope M, Haase A (2003). "Transmission, acute HIV-1 infection and the quest for strategies to prevent infection". Nat Med. 9 (7): 847–52. doi:10.1038/nm0703-847. PMID 12835704.
- ↑ Haedicke, J.; Brown, C.; Naghavi, M. H. (2009). "The brain-specific factor FEZ1 is a determinant of neuronal susceptibility to HIV-1 infection". Proceedings of the National Academy of Sciences. 106 (33): 14040–14045. doi:10.1073/pnas.0900502106. ISSN 0027-8424.
- ↑ 99.0 99.1 99.2 Zheng, Y. H., Lovsin, N. and Peterlin, B. M. (2005). "Newly identified host factors modulate HIV replication". Immunol. Lett. 97 (2): 225–34. doi:10.1016/j.imlet.2004.11.026. PMID 15752562.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Doc Kaiser's Microbiology Home Page > IV. VIRUSES > F. ANIMAL VIRUS LIFE CYCLES > 3. The Life Cycle of HIV Naka-arkibo 2010-07-26 sa Wayback Machine. Community College of Baltimore County. Updated: Jan., 2008
- ↑ Hiscott J, Kwon H, Genin P. (2001). "Hostile takeovers: viral appropriation of the NF-kB pathway". J Clin Invest. 107 (2): 143–151. doi:10.1172/JCI11918. PMC 199181. PMID 11160127.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Pollard, V. W. and Malim, M. H. (1998). "The HIV-1 Rev protein". Annu. Rev. Microbiol. 52: 491–532. doi:10.1146/annurev.micro.52.1.491. PMID 9891806.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Gelderblom, H. R (1997). "Fine structure of HIV and SIV" (PDF). In Los Alamos National Laboratory (ed.) (pat.). HIV Sequence Compendium (PDF). Los Alamos, New Mexico: Los Alamos National Laboratory. pp. 31–44.
{{cite book}}:|editor=has generic name (tulong);|format=requires|url=(tulong); Unknown parameter|chapterurl=ignored (|chapter-url=suggested) (tulong) - ↑ 104.0 104.1 104.2 104.3 Robertson DL, Hahn BH, Sharp PM. (1995). "Recombination in AIDS viruses". J Mol Evol. 40 (3): 249–59. doi:10.1007/BF00163230. PMID 7723052.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Rambaut, A; Posada, D; Crandall, KA; Holmes, EC; et al. (2004). "The causes and consequences of HIV evolution". Nature Reviews Genetics. 5 (52–61): 52–61. doi:10.1038/nrg1246. PMID 14708016. Inarkibo mula sa ang orihinal noong 2019-11-09. Nakuha noong 2012-08-18.
{{cite journal}}: Explicit use of et al. in:|first=(tulong); Unknown parameter|month=ignored (tulong) - ↑ Perelson AS, Ribeiro RM (2008). "Estimating drug efficacy and viral dynamic parameters: HIV and HCV". Stat Med. 27 (23): 4647–57. doi:10.1002/sim.3116. PMID 17960579.
{{cite journal}}: Unknown parameter|month=ignored (tulong) - ↑ 107.0 107.1 PMID 19661993 (PubMed)
Citation will be completed automatically in a few minutes. Jump the queue or expand by hand - ↑ Holzammer S, Holznagel E, Kaul A, Kurth R, Norley S (2001). "High virus loads in naturally and experimentally SIVagm-infected African green monkeys". Virology. 283 (2): 324–31. doi:10.1006/viro.2001.0870. PMID 11336557.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Kurth, R. and Norley, S. (1996). "Why don't the natural hosts of SIV develop simian AIDS?". J. NIH Res. 8: 33–37.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Baier M, Dittmar MT, Cichutek K, Kurth R (1991). "Development of vivo of genetic variability of simian immunodeficiency virus". Proc. Natl. Acad. Sci. U.S.A. 88 (18): 8126–30. Bibcode:1991PNAS...88.8126B. doi:10.1073/pnas.88.18.8126. PMC 52459. PMID 1896460.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Daniel MD, King NW, Letvin NL, Hunt RD, Sehgal PK, Desrosiers RC (1984). "A new type D retrovirus isolated from macaques with an immunodeficiency syndrome". Science. 223 (4636): 602–5. Bibcode:1984Sci...223..602D. doi:10.1126/science.6695172. PMID 6695172.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ 112.0 112.1 PMID 19626114 (PubMed)
Citation will be completed automatically in a few minutes. Jump the queue or expand by hand - ↑
Thomson, M. M., Perez-Alvarez, L. and Najera, R. (2002). "Molecular epidemiology of HIV-1 genetic forms and its significance for vaccine development and therapy". Lancet Infect. Dis. 2 (8): 461–471. doi:10.1016/S1473-3099(02)00343-2. PMID 12150845.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Carr, J. K. (1998). "Reference Sequences Representing the Principal Genetic Diversity of HIV-1 in the Pandemic" (PDF). In Los Alamos National Laboratory (ed.) (pat.). HIV Sequence Compendium (PDF). Los Alamos, New Mexico: Los Alamos National Laboratory. pp. 10–19.
{{cite book}}:|editor=has generic name (tulong);|format=requires|url=(tulong); Unknown parameter|chapterurl=ignored (|chapter-url=suggested) (tulong); Unknown parameter|coauthors=ignored (|author=suggested) (tulong) - ↑
Osmanov S, Pattou C, Walker N, Schwardlander B, Esparza J; WHO-UNAIDS Network for HIV Isolation and Characterization. (2002). "Estimated global distribution and regional spread of HIV-1 genetic subtypes in the year 2000". Acquir. Immune. Defic. Syndr. 29 (2): 184–190. PMID 11832690.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑
Perrin L, Kaiser L, Yerly S. (2003). "Travel and the spread of HIV-1 genetic variants". Lancet Infect Dis. 3 (1): 22–27. doi:10.1016/S1473-3099(03)00484-5. PMID 12505029.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ 117.0 117.1 Plantier JC, Leoz M, Dickerson JE; et al. (2009). "A new human immunodeficiency virus derived from gorillas". Nat. Med. 15 (8): 871–2. doi:10.1038/nm.2016. PMID 19648927.
{{cite journal}}: Explicit use of et al. in:|author=(tulong); Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Smith, L (2009-08-03). "Woman found carrying new strain of HIV from gorillas". London: The Independent. Inarkibo mula sa ang orihinal noong 2012-12-24. Nakuha noong 2009-08-04.
- ↑ "Gorillas may be a source of AIDS, researchers find". Reuters India. 2009-08-03. Inarkibo mula sa ang orihinal noong 2009-09-09. Nakuha noong 2009-08-04.
- ↑ May, MT; Ingle, SM (2011 Dec). "Life expectancy of HIV-positive adults: a review". Sexual health. 8 (4): 526–33. doi:10.1071/SH11046. PMID 22127039.
{{cite journal}}: Check date values in:|date=(tulong) - ↑ 121.0 121.1 121.2 121.3 121.4 121.5 121.6 121.7 Antiretroviral therapy for HIV infection in adults and adolescents: recommendations for a public health approach (PDF). World Health Organization. 2010. pp. 19–20. ISBN 978-92-4-159976-4.
- ↑ 122.00 122.01 122.02 122.03 122.04 122.05 122.06 122.07 122.08 122.09 122.10 Vogel, M; Schwarze-Zander, C; Wasmuth, JC; Spengler, U; Sauerbruch, T; Rockstroh, JK (2010 Jul). "The treatment of patients with HIV". Deutsches Ärzteblatt international. 107 (28–29): 507–15, quiz 516. doi:10.3238/arztebl.2010.0507. PMC 2915483. PMID 20703338.
{{cite journal}}: Check date values in:|date=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Sax, PE; Baden, LR (2009-04-30). "When to start antiretroviral therapy—ready when you are?". The New England Journal of Medicine. 360 (18): 1897–9. doi:10.1056/NEJMe0902713. PMID 19339713.
- ↑ Siegfried, N; Uthman, OA; Rutherford, GW (2010-03-17). Siegfried, Nandi (pat.). "Optimal time for initiation of antiretroviral therapy in asymptomatic, HIV-infected, treatment-naive adults". Cochrane database of systematic reviews (Online) (3): CD008272. doi:10.1002/14651858.CD008272.pub2. PMID 20238364.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Panel on Antiretroviral Guidelines for Adults and Adolescents (2009-12-01). Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents (PDF). United States Department of Health and Human Services. p. i. Inarkibo mula sa ang orihinal (PDF) noong 2009-01-13. Nakuha noong 2012-08-27.
- ↑ When To Start, Consortium; Sterne, JA; May, M; Costagliola, D; de Wolf, F; Phillips, AN; Harris, R; Funk, MJ; Geskus, RB; Gill, J; Dabis, F; Miró, JM; Justice, AC; Ledergerber, B; Fätkenheuer, G; Hogg, RS; Monforte, AD; Saag, M; Smith, C; Staszewski, S; Egger, M; Cole, SR (2009-04-18). "Timing of initiation of antiretroviral therapy in AIDS-free HIV-1-infected patients: a collaborative analysis of 18 HIV cohort studies". Lancet. 373 (9672): 1352–63. doi:10.1016/S0140-6736(09)60612-7. PMC 2670965. PMID 19361855.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Beard, J; Feeley, F; Rosen, S (2009 Nov). "Economic and quality of life outcomes of antiretroviral therapy for HIV/AIDS in developing countries: a systematic literature review". AIDS care. 21 (11): 1343–56. doi:10.1080/09540120902889926. PMID 20024710.
{{cite journal}}: Check date values in:|date=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Orrell, C (2005 Nov). "Antiretroviral adherence in a resource-poor setting". Current HIV/AIDS reports. 2 (4): 171–6. doi:10.1007/s11904-005-0012-8. PMID 16343374.
{{cite journal}}: Check date values in:|date=(tulong) - ↑ Malta, M; Strathdee, SA; Magnanini, MM; Bastos, FI (2008 Aug). "Adherence to antiretroviral therapy for human immunodeficiency virus/acquired immune deficiency syndrome among drug users: a systematic review". Addiction (Abingdon, England). 103 (8): 1242–57. doi:10.1111/j.1360-0443.2008.02269.x. PMID 18855813.
{{cite journal}}: Check date values in:|date=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Nachega, JB; Marconi, VC; van Zyl, GU; Gardner, EM; Preiser, W; Hong, SY; Mills, EJ; Gross, R (2011 Apr). "HIV treatment adherence, drug resistance, virologic failure: evolving concepts". Infectious disorders drug targets. 11 (2): 167–74. PMID 21406048.
{{cite journal}}: Check date values in:|date=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Nachega, JB; Mills, EJ; Schechter, M (2010 Jan). "Antiretroviral therapy adherence and retention in care in middle-income and low-income countries: current status of knowledge and research priorities". Current opinion in HIV and AIDS. 5 (1): 70–7. doi:10.1097/COH.0b013e328333ad61. PMID 20046150.
{{cite journal}}: Check date values in:|date=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ 132.0 132.1 132.2 Montessori, V., Press, N., Harris, M., Akagi, L., Montaner, J. S. (2004). "Adverse effects of antiretroviral therapy for HIV infection". CMAJ. 170 (2): 229–238. PMC 315530. PMID 14734438.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Mandell, Bennett, and Dolan (2010). Chapter 121.
- ↑ Burgoyne RW, Tan DH (2008). "Prolongation and quality of life for HIV-infected adults treated with highly active antiretroviral therapy (HAART): a balancing act". J. Antimicrob. Chemother. 61 (3): 469–73. doi:10.1093/jac/dkm499. PMID 18174196.
{{cite journal}}: Unknown parameter|month=ignored (tulong) - ↑ Barbaro, G; Barbarini, G (2011 Dec). "Human immunodeficiency virus & cardiovascular risk". The Indian journal of medical research. 134 (6): 898–903. doi:10.4103/0971-5916.92634. PMC 3284097. PMID 22310821.
{{cite journal}}: Check date values in:|date=(tulong) - ↑ Orsi, F; d'almeida, C (2010 May). "Soaring antiretroviral prices, TRIPS and TRIPS flexibilities: a burning issue for antiretroviral treatment scale-up in developing countries". Current opinion in HIV and AIDS. 5 (3): 237–41. doi:10.1097/COH.0b013e32833860ba. PMID 20539080.
{{cite journal}}: Check date values in:|date=(tulong) - ↑ 137.0 137.1 UNAIDS 2011 pg. 150–160
- ↑ 138.0 138.1 "Guidelines for the Use of Antiretroviral Agents in Pediatric HIV Infection" (PDF). The Panel on Antiretroviral Therapy and Medical Management of HIV-Infected Children. 11 Agosto 2011. Inarkibo mula sa ang orihinal (PDF) noong 16 Pebrero 2013. Nakuha noong 27 Agosto 2012.
- ↑ Antiretroviral therapy for HIV infection in infants and children (PDF). World Health Organization. 2010. p. 2. ISBN 978-92-4-159980-1. Inarkibo mula sa ang orihinal (PDF) noong 2014-02-24. Nakuha noong 2012-08-27.
- ↑ Laurence J (2006). "Hepatitis A and B virus immunization in HIV-infected persons". AIDS Reader. 16 (1): 15–17. PMID 16433468.
- ↑ Huang, L; Cattamanchi, A; Davis, JL; den Boon, S; Kovacs, J; Meshnick, S; Miller, RF; Walzer, PD; Worodria, W; Masur, H; International HIV-associated Opportunistic Pneumonias (IHOP), Study; Lung HIV, Study (2011 Jun). "HIV-associated Pneumocystis pneumonia". Proceedings of the American Thoracic Society. 8 (3): 294–300. doi:10.1513/pats.201009-062WR. PMC 3132788. PMID 21653531.
{{cite journal}}: Check date values in:|date=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ "Treating opportunistic infections among HIV-infected adults and adolescents. Recommendations from CDC, the National Institutes of Health, and the HIV Medicine Association/Infectious Diseases Society of America". Department of Health and Human Services. 2 Pebrero 2007. Inarkibo mula sa ang orihinal noong 2012-12-12. Nakuha noong 2012-08-27. Naka-arkibo 2013-03-21 sa Wayback Machine.
- ↑ Smith, [edited by] Blaine T. (2008). Concepts in immunology and immunotherapeutics (4th pat.). Bethesda, Md.: American Society of Health-System Pharmacists. p. 143. ISBN 978-1-58528-127-5.
{{cite book}}:|first=has generic name (tulong) - ↑ Littlewood RA, Vanable PA (2008). "Complementary and alternative medicine use among HIV-positive people: research synthesis and implications for HIV care". AIDS Care. 20 (8): 1002–18. doi:10.1080/09540120701767216. PMC 2570227. PMID 18608078.
{{cite journal}}: Unknown parameter|month=ignored (tulong) - ↑ Mills E, Wu P, Ernst E (2005). "Complementary therapies for the treatment of HIV: in search of the evidence". Int J STD AIDS. 16 (6): 395–403. doi:10.1258/0956462054093962. PMID 15969772.
{{cite journal}}: Unknown parameter|month=ignored (tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ 146.0 146.1 146.2 Irlam, JH; Visser, MM; Rollins, NN; Siegfried, N (2010-12-08). Irlam, James H (pat.). "Micronutrient supplementation in children and adults with HIV infection". Cochrane database of systematic reviews (Online) (12): CD003650. doi:10.1002/14651858.CD003650.pub3. PMID 21154354.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link) - ↑ Stone, CA; Kawai, K; Kupka, R; Fawzi, WW (2010 Nov). "Role of selenium in HIV infection". Nutrition Reviews. 68 (11): 671–81. doi:10.1111/j.1753-4887.2010.00337.x. PMC 3066516. PMID 20961297.
{{cite journal}}: Check date values in:|date=(tulong)CS1 maint: multiple names: mga may-akda (link) - ↑ Forrester, JE; Sztam, KA (2011 Dec). "Micronutrients in HIV/AIDS: is there evidence to change the WHO 2003 recommendations?". The American journal of clinical nutrition. 94 (6): 1683S–1689S. doi:10.3945/ajcn.111.011999. PMC 3226021. PMID 22089440.
{{cite journal}}: Check date values in:|date=(tulong) - ↑ 149.0 149.1 World Health Organization (2003–05). Nutrient requirements for people living with HIV/AIDS: Report of a technical consultation (PDF). Geneva. Inarkibo (PDF) mula sa orihinal noong 2009-03-25. Nakuha noong 31 Marso 2009.
{{cite book}}: Check date values in:|date=(tulong); Unknown parameter|deadurl=ignored (|url-status=suggested) (tulong) - ↑ Liu JP, Manheimer E, Yang M (2005). Liu, Jian Ping (pat.). "Herbal medicines for treating HIV infection and AIDS". Cochrane Database Syst Rev (3): CD003937. doi:10.1002/14651858.CD003937.pub2. PMID 16034917.
{{cite journal}}: CS1 maint: multiple names: mga may-akda (link)